题目内容
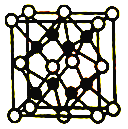
【题目】A、B、C、D四种物质之间的转化关系如图所示(部分产物已略去),下列说法正确的是( )

A. 若A为AlCl3溶液,B可能为氨水,反应①的离子方程式为:A13++4NH3·H2O=AlO2+ 4NH4++2H2O
B. 若A为Fe,B可能为稀硝酸,反应②的离子方程式为: 3Fe+8H++2NO3=3Fe2++2NO↑+4H2O
C. 若A为NaOH溶液,B可能为CO2,可用Ca(OH)2溶液鉴别C、D溶液
D. 若A为Cl2,B可能为NH3,实验室可用加热固体C的方法制取NH3
【答案】B
【解析】A. 氯化铝与氨水反应,与氨水的量的多少无关,过量的氨水不能溶解生成的氢氧化铝沉淀,故A错误;B. 铁与稀硝酸反应与量有关,硝酸过量,将铁氧化为铁离子,硝酸不足,反应生成亚铁离子,若A为Fe,B可能为稀HNO3,此时反应②的离子方程式为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故B正确;C. 若A为NaOH溶液,B可能为CO2,C为碳酸氢钠,D为碳酸钠,二者与Ca(OH)2溶液均生成白色沉淀,无法区分,故C错误;D. 若A为Cl2,B为NH3,则C为氯化铵,D为氯化氢,加热固体氯化铵分解生成氨气和氯化氢,氨气和氯化氢又化合生成氯化铵,不能用来制取NH3,故D错误;故选B。

【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HC1O |
电离平衡常数 | 1.7×10-5 | K1=4.3×10 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)CH3COOH、H2CO3、HC1O的酸性由强到弱的顺序为______________________。
(2)写出H2CO3的电离方程式:______________________。
(3)常温下0.1 mol·L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是______________________(填宇母序号,下同)。
A.c(H+) B.c(H+)/c(CH3COOH)
C. c(H+)·c(OH-) D. 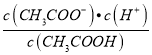
若该溶液升髙温度,上述4种表达式的数据增大的是_________________________。
(4)取0.10mol CH3COOH (冰醋酸)作导电性实验,测得其导电率随加入的水量变化如图所示:比较a、b点的相关性质(填“>”“<”或“=”):
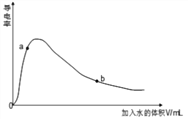
n(H+)∶a_____b;c(CH3COO-)∶a_____b;完全中和时消耗NaOH的物质的量∶a_____b;
(5)H+浓度相同等体积的两份溶液A(盐酸)和B(CH3COOH)分別与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同, 则下列说法正确的是__________(填写序号)
①反应所需要的时间B>A ②开始反应时的速率A>B
③参加反应的锌的物质的量A=B ④A中有锌剩余