题目内容
12.利用如图所示装置进行下列实验,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 | 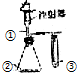 |
| A | 稀盐酸 | Na2SO4 | 溴水 | SO2具有漂白性 | |
| B | 浓氨水 | CaO | AlCl3溶液 | 白色沉淀生成后又溶解 | |
| C | 双氧水 | MnO2 | KI溶液 | 氧化性:O2>I2 | |
| D | 稀醋酸 | Na2CO3 | Na2SiO3溶液 | 酸性:醋酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二氧化硫具有还原性,能被强氧化剂氧化;
B.氢氧化铝具有两性,能溶于强酸、强碱溶液,但不溶于弱碱溶液;
C.同一氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性;
D.乙酸也能和硅酸钠反应生成硅酸沉淀.
解答 解:A.二氧化硫具有还原性,溴具有强氧化性,在水溶液中,二者发生氧化还原反应生成硫酸和HBr,该反应中二氧化硫体现还原性,故A错误;
B.氢氧化铝具有两性,能溶于强酸、强碱溶液,但不溶于弱碱溶液,氨水属于弱碱溶液,所以生成的氢氧化铝沉淀不溶解,则结论错误,故B错误;
C.双氧水分解生成氧气,氧气能氧化碘离子生成碘,碘离子和氧气反应中氧气是氧化剂、碘是氧化产物,所以氧化性O2>I2,故C正确;
D.醋酸和碳酸钠反应生成二氧化碳,且该反应是放热反应,放出的热量促进乙酸挥发,所以得到的二氧化碳中含有乙酸,乙酸也能和硅酸钠反应生成硅酸沉淀,对二氧化碳和硅酸钠的反应造成干扰,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及酸性强弱判断、氧化性强弱比较、氢氧化铝的两性等知识点,明确物质的性质及实验原理是解本题关键,易错选项是D,注意乙酸的干扰.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
2.下列反应的能量变化情况符合如图的是( )
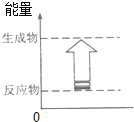

| A. | 石灰石在高温下的分解反应 | B. | 金属钠和水的反应 | ||
| C. | 盐酸与氢氧化钠溶液的反应 | D. | 木炭在氧气中燃烧 |
3.下面有关丙烷、丙烯、丙炔说法中正确的是( )
| A. | 如图,丙烷、丙烯、丙炔的结构分别表示为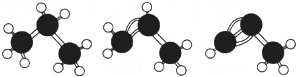 | |
| B. | 相同物质的量的三种物质完全燃烧,生成的气体在标准状态下,体积比3:2:1 | |
| C. | 丙烷、丙烯、丙炔三种物质的熔沸点逐渐升高,相同条件下密度逐渐增大 | |
| D. | 丙炔的碳原予空间结构呈线性排列 |
20.下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S ②还原性:HI>HBr>HCl
③熔沸点:SiO2>Na>NaCl>CO2 ④酸性:HNO3>H2CO3>HClO.
①热稳定性:H2O>HF>H2S ②还原性:HI>HBr>HCl
③熔沸点:SiO2>Na>NaCl>CO2 ④酸性:HNO3>H2CO3>HClO.
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
7.下列分子式表示的有机物可能是混合物的是( )
| A. | C6H6 | B. | C2H6 | C. | C3H8 | D. | C2H5Cl |
8.氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等.下列反应与Br2+SO2+2H2O=H2SO2+2HBr相比较,水的作用相同的是( )
| A. | 电解水:2H20=2H2↑+O2↑ | B. | 4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||
| C. | 2F2+H2O=4HF+O2 | D. | 3NO2+H2O=2HNO3+NO |



