题目内容
10.X、Y、Z、W在周期表中的相对位置如图所示,其中X是地壳中含量最多的元素,下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X | |
| B. | W氢化物的沸点比X氢化物的沸点高 | |
| C. | Y元素的周期序数等于主族序数 | |
| D. | Y、Z两元素的最高价氧化物对应的水化物能发生化学反应 |
分析 这几种都是短周期元素,X是地壳中含量最多的元素,则X为O元素,由元素在周期表中的相对位置,可知Y为Na,Z为Al,W为Cl,据此解答.
解答 解:这几种都是短周期元素,X是地壳中含量最多的元素,则X为O元素,由元素在周期表中的相对位置,可知Y为Na,Z为Al,W为Cl.
A.同周期随原子序数增大原子半径减小,同主族自上而下原子半径增大,故原子半径:Y>Z>W>X,故A错误;
B.W、X的氢化物分别为硫化氢、水,水分子之间存在氢键,沸点高于硫化氢,故B错误;
C.Y为Na元素,处于第三周期IA族,其周期序数不等于主族序数,故C错误;
D.Y、Z的最高价氧化物对应水化物分别为氢氧化钠、氢氧化铝,二者反应生成偏铝酸钠与水,故D正确,
故选D.
点评 本题考查元素周期表与元素周期律,比较基础,注意氢键对物质性质的影响.

练习册系列答案
相关题目
20.据报导用激光将置于铁室中的石墨靶上的碳原子“炸松”,与此同时再用一个射频电火花喷射出氮气,此时碳、氮原子结合成碳氮化合物的薄膜,该膜的硬度可比金刚石更坚硬,其原因可能是( )
| A. | 碳、氮原子构成网状的原子晶体 | |
| B. | 膜中的C-N键长比金刚石的C-C键长短 | |
| C. | 碳、氮都是非金属,化合时放出大量热 | |
| D. | 相邻主族非金属的化合物比单质硬度大 |
1.下列说法正确的是( )
| A. | 实验时酸或碱溅到眼中,应立即用水冲洗,并不断眨眼,不能用手搓揉眼睛 | |
| B. | 检验硫酸亚铁铵溶液中Fe2+的方法是:先滴加新制氨水后滴加KSCN溶液 | |
| C. | 证明钢铁吸收氧腐蚀的方法是:在镀锌铁皮上滴1~3滴含酚酞的饱和食盐水,静置1~2min,观察现象 | |
| D. | 用新制氢氧化铜悬浊液不能鉴别乙醇溶液和葡萄糖溶液 |
5.下列有关溶液中微粒的物质的量浓度关系不正确的是( )
| A. | 0.1 mol•L-1CH3COONa溶液与0.1 mol•L-1HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-) | |
| B. | 0.1 mol•L-1NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol•L-1Na2CO3溶液与0.1 mol•L-1NaHCO3溶液等体积混合:$\frac{2}{3}$c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 0.1 mol•L-1Na2C2O4溶液与0.1 mol•L-1HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+). |
15.化学与能源开发、环境保护、资源利用等密切相关,下列说法正确的是( )
| A. | 硅酸钠的水溶液俗称水玻璃,可用作木材防火剂 | |
| B. | 开发核能、太阳能等新能,推广甲醇汽油,使用无磷洗涤剂都可直接降低碳排放 | |
| C. | 用聚合硫酸铁作为净水剂,该处理过程中仅发生了化学变化 | |
| D. | 汽车尾气中含有氮的氧化物,是汽油不完全燃烧造成的 |
2.H、Al、O、N、S是常见的六种元素
(1)S位于元素周期表三周期第VIA族,Fe的基态原子核外价电子排布式为3d64s2(或1s22s22p63s23p63d64s2);O的基态原子核外有8种运动状态不同的电子
(2)用“>”“<”或“=”填空
(3)己知:下列两个热化学方程式:
4Fe(s)+302(g)=2Fe2O3(s)△H=-aKJ/mol
4Al(s)+3O2(g)=2Al2O3(S)△H=-bKJ/mol
則Al(s)的单质和Fe2O3(s)反应的热化学方程式是Fe2O3(s)+2Al(s)=Al2O3(s)+2Fe(s)△H=-$\frac{1}{2}$(b-a)KJ•mol-1
(4)FeSO4溶液可与硝酸发生反应,写出此反应的离子方程式,并标出电子转移的方向和数目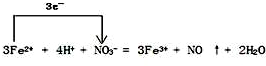 .
.
(1)S位于元素周期表三周期第VIA族,Fe的基态原子核外价电子排布式为3d64s2(或1s22s22p63s23p63d64s2);O的基态原子核外有8种运动状态不同的电子
(2)用“>”“<”或“=”填空
| 第一电离能 | 氧化性 | 沸点 | 非金属性 |
| N>S | Fe3+>Al3+ | NH3<H2O | 16O=18O |
4Fe(s)+302(g)=2Fe2O3(s)△H=-aKJ/mol
4Al(s)+3O2(g)=2Al2O3(S)△H=-bKJ/mol
則Al(s)的单质和Fe2O3(s)反应的热化学方程式是Fe2O3(s)+2Al(s)=Al2O3(s)+2Fe(s)△H=-$\frac{1}{2}$(b-a)KJ•mol-1
(4)FeSO4溶液可与硝酸发生反应,写出此反应的离子方程式,并标出电子转移的方向和数目
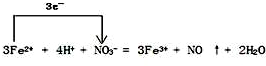 .
.
19.美国康乃尔大学的魏考克斯(C.Wilxox)所合成的一种有机分子,就像一尊释迦牟尼佛.因而称为释迦牟尼分子(所有原子在同一平面).有关该有机物分子的说法不正确的是( )

| A. | 该有机物属于苯的同系物 | |
| B. | 1mol该有机物完全燃烧需消耗25molO2 | |
| C. | 该有机物分子中含有21个碳原子 | |
| D. | 该有机物的一氯代物只有6种 |