题目内容
17.有NO、CO2、NO2三种气体,它们分别都含有0.5mol氧原子,同温同压下三种气体的体积之比为( )| A. | 1:2:3 | B. | 2:1:1 | C. | 4:2:1 | D. | 1:2:4 |
分析 都含有0.5mol氧原子,结合构成可知,NO、CO2、NO2三种气体的物质的量分别为0.5mol、0.25mol、0.25mol,结合相同条件下气体体积之比等于物质的量比来解答.
解答 解:都含有0.5mol氧原子,结合构成可知,NO、CO2、NO2三种气体的物质的量分别为0.5mol、0.25mol、0.25mol,
又相同条件下气体体积之比等于物质的量比,
所以同温同压下三种气体的体积之比为0.5mol:0.25mol:0.25mol=2:1:1,
故选B.
点评 本题考查综合物质的量的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握分子构成及阿伏伽德罗定律的运用,题目难度不大.

练习册系列答案
相关题目
5.下列物质分类正确的是( )
| A. | HCl、纯碱、硫酸钡均为强电解质 | |
| B. | SO2、SiO2、CO均为酸性氧化物 | |
| C. | 稀豆浆、油水、氯化铁溶液均为胶体 | |
| D. | 大理石、CuSO4•5H2O、氨水均为混合物 |
2.在光照条件下,将等物质的量的甲烷和氯气充分反应,所得产物中物质的量最多的是( )
| A. | CH3Cl | B. | CH2Cl2 | C. | CHCl3 | D. | HCl |
9.下列关于胶体的说法中不正确的是( )
| A. | 胶体外观不均一 | B. | 胶体能产生丁达尔效应 | ||
| C. | 胶体能透过滤纸 | D. | 胶体粒子直径在1-100 nm之间 |
6.加入KOH溶液后,下列溶液中哪种离子数目会减少( )
| A. | CO32- | B. | Mg2+ | C. | SO42- | D. | Na+ |
7.检验Na2CO3溶液含有的Cl-和SO${\;}_{4}^{2-}$时,选用的试剂及加入的先后次序是( )
| A. | HCl、BaCl2、AgNO3 | B. | AgNO3、HNO3、Ba(NO3)2 | ||
| C. | HNO3、Ba(NO3)2、AgNO3 | D. | AgNO3、HC1、BaC12 |

 Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.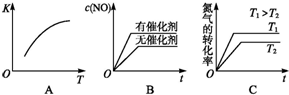 汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)?2NO(g)△H>0已知该反应在2404℃时,平衡常数K=64×10-4.请回答:
汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)?2NO(g)△H>0已知该反应在2404℃时,平衡常数K=64×10-4.请回答: