题目内容
100 g炭粉燃烧所得气体中,CO占 、CO2占
、CO2占 ,且C(s)+
,且C(s)+ O2(g)=CO(g) ΔH=-110.35 kJ·mol-1,CO(g)+
O2(g)=CO(g) ΔH=-110.35 kJ·mol-1,CO(g)+ O2(g)=CO2(g) ΔH=-282.57 kJ·mol-1,与这些炭粉完全燃烧相比损失的热量是 ( )。
O2(g)=CO2(g) ΔH=-282.57 kJ·mol-1,与这些炭粉完全燃烧相比损失的热量是 ( )。
 、CO2占
、CO2占 ,且C(s)+
,且C(s)+ O2(g)=CO(g) ΔH=-110.35 kJ·mol-1,CO(g)+
O2(g)=CO(g) ΔH=-110.35 kJ·mol-1,CO(g)+ O2(g)=CO2(g) ΔH=-282.57 kJ·mol-1,与这些炭粉完全燃烧相比损失的热量是 ( )。
O2(g)=CO2(g) ΔH=-282.57 kJ·mol-1,与这些炭粉完全燃烧相比损失的热量是 ( )。| A.784.92 kJ | B.2 489.44 kJ | C.1 569.83 kJ | D.3 274.3 kJ |
C
损失的热量即为生成的CO没有再燃烧的热量,故损失的热量为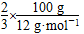 ×282.57 kJ·mol-1=1 569.83 kJ,C项正确。
×282.57 kJ·mol-1=1 569.83 kJ,C项正确。
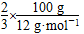 ×282.57 kJ·mol-1=1 569.83 kJ,C项正确。
×282.57 kJ·mol-1=1 569.83 kJ,C项正确。
练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目

 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据: 2NH3(g) △H<0。现将10 mol N2和26 mol H2置于容积可变的密闭容器中,N2的平衡转化率(
2NH3(g) △H<0。现将10 mol N2和26 mol H2置于容积可变的密闭容器中,N2的平衡转化率( )与体系总压强(P)、温度(T)的关系如图所示。回答下列问题:
)与体系总压强(P)、温度(T)的关系如图所示。回答下列问题:
 CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为 。
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为 。 2SO3(g) ΔH="-Q" kJ·mol-1。向一密闭容器中加入2 mol SO2和1 mol O2,达平衡时SO2的转化率为90%,放出的热量为Q1 kJ;向另一相同容器中加入2 mol SO3,在相同条件下,达平衡时吸收的热量为Q2 kJ,则下列关系中正确的是( )
2SO3(g) ΔH="-Q" kJ·mol-1。向一密闭容器中加入2 mol SO2和1 mol O2,达平衡时SO2的转化率为90%,放出的热量为Q1 kJ;向另一相同容器中加入2 mol SO3,在相同条件下,达平衡时吸收的热量为Q2 kJ,则下列关系中正确的是( ) 2SO3(g)
2SO3(g) 
