题目内容
16.如表为元素周期表的一部分,參照元素①-⑤在表中的位置,下列判断正确的是( )| 族 周期 | IA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ||||
| A. | 金属性③>② | B. | ④原子核外有4个电子层 | ||
| C. | 原子半径⑤>③ | D. | 元素①④最高化合价相等 |
分析 由元素在周期表中位置,可知①为C、②为Na、③为Al、④为Si、⑤为Cl.
A.同周期自左而右元素金属性减弱;
B.电子层数等于周期数;
C.同周期自左而右原子半径减小;
D.主族元素最高正化合价等于主族族序数.
解答 解:由元素在周期表中位置,可知①为C、②为Na、③为Al、④为Si、⑤为Cl.
A.同周期自左而右元素金属性减弱,故金属性③<②,故A错误;
B.④位于第三周期,原子核外有3个电子层,故B错误;
C.同周期自左而右原子半径减小,故原子半径:⑤<③,故C错误;
D.元素①④处于ⅣA族,最高化合价均为+4,故D正确,
故选:D.
点评 本题考查元素周期表与元素周期律,侧重对元素周期律的考查,有利于基础知识的巩固.

练习册系列答案
相关题目
6.某500mL溶液中含0.1mol Fe2+、0.2mol Fe3+,加入0.2mol铁粉,待Fe3+完全还原后,溶液中Fe2+的物质的量浓度为(假设反应前后体积不变)( )
| A. | 0.4 mol•L-1 | B. | 0.6 mol•L-1 | C. | 0.8 mol•L-1 | D. | 1.0 mol•L-1 |
4.下列不能用勒夏特列原理解释的是( )
| A. | Fe(SCN)3溶液中加入固体KSCN后颜色变深 | |
| B. | 棕红色NO2加压后颜色先变深后变浅 | |
| C. | SO2催化氧化成SO3的反应,往往需要使用催化剂 | |
| D. | FeCl3溶液的配制需先将固体FeCl3溶解在盐酸中,再加水稀释到相应浓度 |
11.(1)Ⅰ.短周期某主族元素M的电离能情况如图A所示,则M元素位于周期表的第ⅡA族;
Ⅱ.图B折线c为某主族元素氢化物的沸点的变化规律,呈现这种变化关系的原因是由于N、O、F电负性大,NH3、H2O、HF因在分子间存在多条结合力较大的氢键,总强度远远大于分子间作用力,故沸点高于同主族其它元素氢化物的沸点,只有ⅣA族元素氢化物不存在反常现象.两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:b(填“a”或“b”)
(2)用氢键表示式写出氨水中NH3分子与水分子间形成的可能存在的氢键N-H…O、O-H…N.
(3)下表列出了含氧酸酸性强弱与非羟基氧原子数的关系.
亚磷酸(H3PO3)也是中强酸,则它的结构式为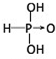 .
.
(4)Cu元素可形成[Cu(NH3)4]SO4,其中存在的化学键类型有①③⑤(填序号).
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键.
Ⅱ.图B折线c为某主族元素氢化物的沸点的变化规律,呈现这种变化关系的原因是由于N、O、F电负性大,NH3、H2O、HF因在分子间存在多条结合力较大的氢键,总强度远远大于分子间作用力,故沸点高于同主族其它元素氢化物的沸点,只有ⅣA族元素氢化物不存在反常现象.两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:b(填“a”或“b”)

(2)用氢键表示式写出氨水中NH3分子与水分子间形成的可能存在的氢键N-H…O、O-H…N.
(3)下表列出了含氧酸酸性强弱与非羟基氧原子数的关系.
| 次氯酸 | 磷酸 | 硫酸 | 高氧酸 | |
| 含氧酸 | Cl-OH | 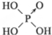 |  | 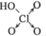 |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
 .
.(4)Cu元素可形成[Cu(NH3)4]SO4,其中存在的化学键类型有①③⑤(填序号).
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键.
1.某学生实验小组做金属钠与浓盐酸反应实验,发现反应平稳,无火星,有白雾,有大量的白色小颗粒向下坠落.对上述实验现象分析不正确的是( )
| A. | 钠在浓盐酸中反应速率比在水中小 | |
| B. | 浓盐酸中c(H+)比稀盐酸中小 | |
| C. | 浓盐酸挥发出大量白雾,使产生的H2无法燃烧和爆炸 | |
| D. | 生成的固体NaCl使反应速率降低 |
8.化学与科学、技术、社会、环境密切相关.下列有关说法中错误的是( )
| A. | 2010年11月广州亚运会燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 | |
| B. | 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶 | |
| C. | 小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 | |
| D. | 青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢铁 |
5.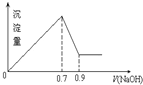 现有AlCl3和Fe2(SO4)3的混合溶液,向其中不断加入 NaOH溶液得到的沉淀的量与加入NaOH溶液的体积的关系如图所示,则原溶液中SO42-与Cl-的物质的量浓度之比为( )
现有AlCl3和Fe2(SO4)3的混合溶液,向其中不断加入 NaOH溶液得到的沉淀的量与加入NaOH溶液的体积的关系如图所示,则原溶液中SO42-与Cl-的物质的量浓度之比为( )
 现有AlCl3和Fe2(SO4)3的混合溶液,向其中不断加入 NaOH溶液得到的沉淀的量与加入NaOH溶液的体积的关系如图所示,则原溶液中SO42-与Cl-的物质的量浓度之比为( )
现有AlCl3和Fe2(SO4)3的混合溶液,向其中不断加入 NaOH溶液得到的沉淀的量与加入NaOH溶液的体积的关系如图所示,则原溶液中SO42-与Cl-的物质的量浓度之比为( )| A. | 3:1 | B. | 1:12 | C. | 3:2 | D. | 6:1 |
6.氧化还原反应前后一定发生变化的是( )
| A. | 原子个数 | B. | 元素种类 | C. | 元素化合价 | D. | 质量 |
