题目内容
6.氧化还原反应前后一定发生变化的是( )| A. | 原子个数 | B. | 元素种类 | C. | 元素化合价 | D. | 质量 |
分析 氧化还原反应中一定存在元素的化合价变化,以此来解答.
解答 解:氧化还原反应的实质为电子转移,其特征为化合价变化,由质量守恒定律可知,化学反应中质量、元素种类、原子个数在反应前后不变,
故选C.
点评 本题考查氧化还原反应,为高频考点,把握氧化还原反应的特征、实质为解答的关键,注意质量守恒定律的理解,题目难度不大.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
16.如表为元素周期表的一部分,參照元素①-⑤在表中的位置,下列判断正确的是( )
| 族 周期 | IA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ||||
| A. | 金属性③>② | B. | ④原子核外有4个电子层 | ||
| C. | 原子半径⑤>③ | D. | 元素①④最高化合价相等 |
17.下列有关物质性质用途叙述正确的是( )
①84消毒液和洁厕灵都显酸性
②Na2CO3、NaHCO3溶液都呈碱性
③配制FeCl3溶液时加入少量的盐酸
④天然气和氢气都是可再生的能源.
①84消毒液和洁厕灵都显酸性
②Na2CO3、NaHCO3溶液都呈碱性
③配制FeCl3溶液时加入少量的盐酸
④天然气和氢气都是可再生的能源.
| A. | ①② | B. | ②③ | C. | ②④ | D. | ③④ |
14.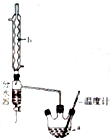 实验室通常以乙醇、乙酸和浓硫酸混合加热制备乙酸乙酯,装置如图所示
实验室通常以乙醇、乙酸和浓硫酸混合加热制备乙酸乙酯,装置如图所示
(1)请用同位素示踪法表示乙酸和乙醇发生酯化反应的反应原理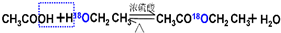
(2)装置中,b的名称为球形冷凝管(冷凝管),其主要作用是冷凝回流;加热前,通常需要在a中加入碎瓷片,目的是防止暴沸
(3)为了证明浓硫酸的作用,某同学进行了以下4个实验,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min,实验结束后测分水器中有机物的厚度,实验记录如表:
①为更好地测定酯层厚度,可预先向饱和Na2CO3溶液中滴加1滴酚酞试液,每次实验结束后可观察到分水器中的现象是液体分层,上层呈无色,下层呈红色
②分析实验A、B、C的数据,可以得出浓硫酸在反应中的作用是催化剂、吸水剂;实验D和实验C对照,你又能得出的结论是对该反应起催化作用的实际上为H+
(4)本实验制备乙酸乙酯的装置与教材装置相比较突出的优点是一是增加了温度计,有利于控制发生装置中反应液的温度,二是增加了冷凝装置,有利于收集产物,三是增加了分水器,能够在反应进行时很容易的把水分离出来,从而使平衡正向移动,提高乙酸乙酯的产率(至少答出两点)
 实验室通常以乙醇、乙酸和浓硫酸混合加热制备乙酸乙酯,装置如图所示
实验室通常以乙醇、乙酸和浓硫酸混合加热制备乙酸乙酯,装置如图所示(1)请用同位素示踪法表示乙酸和乙醇发生酯化反应的反应原理
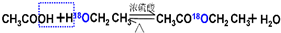
(2)装置中,b的名称为球形冷凝管(冷凝管),其主要作用是冷凝回流;加热前,通常需要在a中加入碎瓷片,目的是防止暴沸
(3)为了证明浓硫酸的作用,某同学进行了以下4个实验,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min,实验结束后测分水器中有机物的厚度,实验记录如表:
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 有机层厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL 18mol•L-1浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 饱和Na2CO3溶液 | 0.1 |
| C | 3mL乙醇、2mL乙酸、6mL 3mol•L-1硫酸 | 饱和Na2CO3溶液 | 1.2 |
| D | 3mL乙醇、2mL乙酸、6mL6mol•L-1盐酸 | 饱和Na2CO3溶液 | 1.2 |
②分析实验A、B、C的数据,可以得出浓硫酸在反应中的作用是催化剂、吸水剂;实验D和实验C对照,你又能得出的结论是对该反应起催化作用的实际上为H+
(4)本实验制备乙酸乙酯的装置与教材装置相比较突出的优点是一是增加了温度计,有利于控制发生装置中反应液的温度,二是增加了冷凝装置,有利于收集产物,三是增加了分水器,能够在反应进行时很容易的把水分离出来,从而使平衡正向移动,提高乙酸乙酯的产率(至少答出两点)
1.用NA表示阿伏加德罗常数值,下列叙述正确的是( )
| A. | 28gCO中含有的分子数为NA | |
| B. | 22.4L空气含有NA个单质分子 | |
| C. | 1mol/L的NaCl溶液含有NA个Na+ | |
| D. | 1mol Na2O2固体中含有的离子总数为4NA |
11.下列离子方程式正确的是( )
| A. | Cu+2H+═Cu2++H2↑ | B. | Na+H2O═Na++2OH-+H2↑ | ||
| C. | NH4++OH-═NH4OH | D. | CaCO3+2H+═Ca2++CO2↑+H2O |
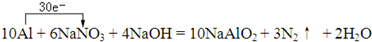
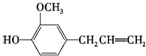 丁子香酚可用作杀虫剂和防腐剂,其结构简式如图:
丁子香酚可用作杀虫剂和防腐剂,其结构简式如图: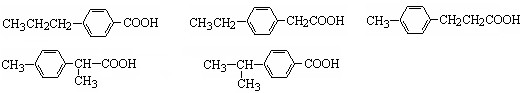 (任意2种)..
(任意2种)..