题目内容
14.如图所示,反应X(g)+3Y(g)?2Z(g),正反应为放热反应,在不同温度、不同压强(p1>p2)下,达到平衡时,混合气体中Z的体积分数中φ(Z)随温度变化的曲线应为( )| A. | 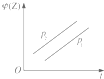 | B. |  | C. | 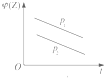 | D. |  |
分析 对于反应X(g)+3Y(g)?2Z(g)△H<0,正反应是体积减小的放热反应,升高温度平衡向逆反应移动,Z的体积φ(Z)减小;增大压强平衡向正反应移动,Z的体积φ(Z)增大,依此进行判断.
解答 解:对于反应X(g)+3Y(g)?2Z(g)△H<0,正反应是体积减小的放热反应,升高温度平衡向逆反应移动,Z的体积φ(Z)减小;增大压强平衡向正反应移动,Z的体积φ(Z)增大,
A.由图象可知,压强一定时,温度越高,Z的体积φ(Z)越大,与实际不符合,故A错误;
B.由图象可知,压强一定时,温度越高,Z的体积φ(Z)越大,与实际不符合,故B错误;
C.由图象可知,压强一定时,温度越高,Z的体积φ(Z)减小;温度一定时,压强越高,Z的体积φ(Z)增大,与实际相符,故C正确;
D.由图象可知,压强一定时,温度越高,Z的体积φ(Z)越小;温度一定时,压强越高,Z的体积φ(Z)减小,与实际不符合,故D错误;
故选C.
点评 本题考查了随温度和压强的变化,生成物浓度的变化,依据勒夏特列原理利用定一议二法分析图象是关键.

练习册系列答案
相关题目
12.化学与环境密切相关.下列有关说法错误的是( )
| A. | CO、NO能与人体的血红蛋白结合,使人中毒 | |
| B. | CaO能与SO2反应,可作工业废气的脱硫剂 | |
| C. | 光化学烟雾会引起呼吸道疾病 | |
| D. | CO2、NO2或SO2都会导致酸雨的形成 |
5.下列物质长期暴露在空气中会变质的是( )
| A. | 浓盐酸 | B. | 浓硫酸 | C. | 食盐 | D. | 氢氧化钠 |
2.研究小组分别用锌片、铝片、Cu和稀硫酸进行原电池的相关的探究,所得部分实验数琚如下,下列说法正确的是( )
| 实验 | 电极甲 | 电极乙 |
| I | Zn | Cu |
| Ⅱ | Al | Cu |
| A. | 两组实验溶液的pH均增大 | |
| B. | 实验Ⅱ中,H+向Al定向迁移 | |
| C. | 实验I中,甲电极反应为:2H++e-=H2↑ | |
| D. | 实验Ⅱ中,电子由铜转移到锌 |
9.下表是元素周期表的一部分,有关说法正确的是 ( )
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | VⅠA | VⅡA |
| 2 | a | b | c | ||||
| 3 | d | e | f | g | h | i |
| A. | a、b、e、f四种元素的原子半径:e>f>b>a | |
| B. | h、i两种元素阴离子的还原性:h>i | |
| C. | a、g两种元素氢化物的稳定性:g>a | |
| D. | d、e、f三种元素最高价氧化物对应的水化物的碱性依次增强 |
19.取三张蓝色石蕊试纸放在玻璃上,然后按顺序滴加65%的HNO3、98.3%H2SO4和新制氯水,三张试纸最后呈现的颜色是( )
| A. | 白、红、白 | B. | 红、黑、红 | C. | 红、红、红 | D. | 白、黑、白 |
6.在Al2(SO4)3、K2SO4、KAl(SO4)2的混合溶液100mL中,如果SO42-的浓度等于0.4mol/L,当加入2mol/L的KOH溶液50mL时,生成沉淀恰好溶解,则原混合物中K+的物质的量浓度是( )
| A. | 0.2mol/L | B. | 0.05mol/L | C. | 0.45mol/L | D. | 0.225mol/L |
4.室温条件下,下列有关溶液中粒子浓度的关系式中,正确的是( )


| A. | 图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH) | |
| B. | pH相同的①CH3COONa、②NaHCO3、③ 三份溶液中的c(Na+):③>②>① 三份溶液中的c(Na+):③>②>① | |
| C. | 图中pH=7时:c(Na+)>c(CH3COO-)>c(OH-)=c(H+) | |
| D. | 图中V(CH3COOH)>20mL,溶液pH<7 |