题目内容
17.某同学在实验报告中有以下实验数据,其中合理的是( )| A. | 用量筒量取5.26ml盐酸 | |
| B. | 用托盘天平称取11.70g食盐 | |
| C. | 用PH试纸测得溶液的PH是3.5 | |
| D. | 用标准NaOH溶液滴定未知浓度的盐酸用去23.10ml NaOH溶液 |
分析 A.量筒准确到0.1mL;
B.托盘天平一般准确到0.1g;
C.广泛pH 试纸只能测得整数值;
D.滴定管的精确度为0.01mL.
解答 解:A.量筒准确到0.1mL,无法量取5.26ml盐酸,故A错误;
B.托盘天平一般准确到0.1g,无法称取11.70g食盐,故B错误;
C.广泛pH 试纸只能测得整数值,不能测得3.5,故C错误;
D.滴定管的精确度为0.01mL,可量取23.10 ml NaOH溶液,故D正确.
故选D.
点评 本题考查化学实验基本操作,难度不大,考虑量筒及托盘天平的最小分度值,托盘天平一般准确到0.1g、10 mL量筒准确到0.1mL、100mL量筒准确到1mL.

练习册系列答案
相关题目
20.下列变化过程中,只发生物理变化的是( )
| A. | 葡萄酿酒 | B. | 酸雨侵蚀建筑物 | ||
| C. | 空气液化制取氮气 | D. | 钢铁生锈 |
5.某烃分子中有两个双键,它的分子式可能是( )
| A. | C4H6 | B. | C7H8 | C. | C5H10 | D. | C10H22 |
2.某不纯的烧碱样品中各成分的质量分数如下表所示:
取a g样品溶于100mL2mol/L的盐酸中,充分反应后,再用适量3mol/LNaOH溶液将剩余的酸恰好中和,最后将溶液蒸干,可得干燥固体的质量为( )
| 成分 | NaOH | Na2CO3 | H2O |
| 质量分数 | 90.4% | 3.8% | 5.8% |
| A. | 11.7 g | B. | 5.85 g | C. | 2.34 g | D. | (2.34-a) g |
9.下列说法中,正确的是( )
| A. | 凡是放热反应都是自发反应 | |
| B. | 凡是熵增大的反应都是自发反应 | |
| C. | 能自发的化学反应就一定能发生并进行完全 | |
| D. | 判断反应进行的方向,应综合考虑体系的焓变和熵变 |
6.下列叙述不正确的是( )
| A. | H2S、H2O、HF的稳定性依次增强 | |
| B. | RbOH、KOH、Mg(OH)2的碱性依次减弱 | |
| C. | Na+、Mg2+、Al3+的氧化性依次减弱 | |
| D. | H2SiO3、H2CO3、H2SO4 酸性依次增强 |
7.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
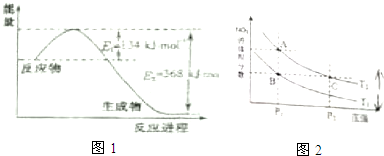
(1)如图1是1mol NO2气体和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2气体和CO反应的热化学方程式NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1.
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0 该反应的化学平衡常数表达式是K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$.已知平衡常数K与温度T的关系如表:
①试判断K1<K2(填写“>”“=”或“<”)
②下列各项能说明该反应已达到平衡状态的是c(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(N2)(正)=3v(H2)(逆)
c.容器内压强保持不变 d.混合气体的密度保持不变
③合成氨在农业和国防中有很重要的意义,在实际工业生产中,常采用下列措施,其中可以用勒夏特列原理解释的是BD(填字母).
A.采用较高温度(400℃~500℃) B.将生成的氨液化并及时从体系中分离出来
C.用铁触媒加快化学反应速率 D.采用较高压强(20MPa~50MPa)
(3)对反应N2O4(g)?2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示,下列说法正确的是CD
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点N2O4的转化率:A<C
d.由状态B到状态A,可以用加热的方法.

(1)如图1是1mol NO2气体和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2气体和CO反应的热化学方程式NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1.
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0 该反应的化学平衡常数表达式是K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$.已知平衡常数K与温度T的关系如表:
| T/℃ | 400 | 300 |
| 平衡常致K | K1 | K2 |
②下列各项能说明该反应已达到平衡状态的是c(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(N2)(正)=3v(H2)(逆)
c.容器内压强保持不变 d.混合气体的密度保持不变
③合成氨在农业和国防中有很重要的意义,在实际工业生产中,常采用下列措施,其中可以用勒夏特列原理解释的是BD(填字母).
A.采用较高温度(400℃~500℃) B.将生成的氨液化并及时从体系中分离出来
C.用铁触媒加快化学反应速率 D.采用较高压强(20MPa~50MPa)
(3)对反应N2O4(g)?2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示,下列说法正确的是CD
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点N2O4的转化率:A<C
d.由状态B到状态A,可以用加热的方法.