题目内容
(12分)2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH1=-99 kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH1=-99 kJ·mol-1

请回答下列问题:
(1)该反应属于________反应(填“放热”或“吸热”)。
(2)图中C表示 。
(3)从化学键的角度分析,F代表什么意义?F ;
(4)改变反应条件可改变E值大小,如加入V2O5作催化剂,可使E值减小。E的大小对该反应的反应热有 。(无影响、有影响、不确定)
(5)图中ΔH=________kJ·mol-1。
(6)若已知1 mol SO2(g)氧化为1 mol SO3(l)的ΔH2=-Q kJ·mol-1,则ΔH1______ΔH2(填“>”、“<”或“=”)。
 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH1=-99 kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH1=-99 kJ·mol-1
请回答下列问题:
(1)该反应属于________反应(填“放热”或“吸热”)。
(2)图中C表示 。
(3)从化学键的角度分析,F代表什么意义?F ;
(4)改变反应条件可改变E值大小,如加入V2O5作催化剂,可使E值减小。E的大小对该反应的反应热有 。(无影响、有影响、不确定)
(5)图中ΔH=________kJ·mol-1。
(6)若已知1 mol SO2(g)氧化为1 mol SO3(l)的ΔH2=-Q kJ·mol-1,则ΔH1______ΔH2(填“>”、“<”或“=”)。
(1)放热 (2)生成物的总能量 (3) 形成新键释放的能量
(4)无影响 (5)-198 (6) >
(4)无影响 (5)-198 (6) >
图像先看清横纵轴:横轴表反应过程,纵轴表物质的能量
(1)分析图像,得:A点表反应物总能量,C点表生成物总能量;反应物总能量高于生成物总能量,故该反应属于放热反应;
(3)B点表过渡态能量,则F为过渡态与产物的能量差,即代表形成新键释放的能量;
(4)E值称为反应的活化能,加催化剂能降低反应的活化能,但不影响该反应
的反应热ΔH;
(5)在热化学方程式中:物质的计量系数表示参加该反应的各物质的物质的量,图中参加反应的SO2为2mol,故ΔH=-99×2kJ·mol-1;
(6)可认为:先1 mol SO2(g)氧化为1 mol SO3(g);再1 mol SO3(g)生成1 mol SO3(l),该反应放热;所以ΔH2的绝对值=ΔH1的绝对值+1 mol SO3(g)生成1 mol SO3(l)时放出的热量,即:ΔH2的绝对值>ΔH1的绝对值,而两者均为负数,则去掉绝对值后,ΔH2<ΔH1;
(1)分析图像,得:A点表反应物总能量,C点表生成物总能量;反应物总能量高于生成物总能量,故该反应属于放热反应;
(3)B点表过渡态能量,则F为过渡态与产物的能量差,即代表形成新键释放的能量;
(4)E值称为反应的活化能,加催化剂能降低反应的活化能,但不影响该反应
的反应热ΔH;
(5)在热化学方程式中:物质的计量系数表示参加该反应的各物质的物质的量,图中参加反应的SO2为2mol,故ΔH=-99×2kJ·mol-1;
(6)可认为:先1 mol SO2(g)氧化为1 mol SO3(g);再1 mol SO3(g)生成1 mol SO3(l),该反应放热;所以ΔH2的绝对值=ΔH1的绝对值+1 mol SO3(g)生成1 mol SO3(l)时放出的热量,即:ΔH2的绝对值>ΔH1的绝对值,而两者均为负数,则去掉绝对值后,ΔH2<ΔH1;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 放出942kJ热量。由此判断下列说法正确的是( )
放出942kJ热量。由此判断下列说法正确的是( )
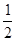 O2(g) = H2O(g) ΔH1=a kJ·mol-1?
O2(g) = H2O(g) ΔH1=a kJ·mol-1? 2NH3(g) △H=a kJ·mol-1。试根据表中所列键能数据估算a 的值: (写出 + 或-)。
2NH3(g) △H=a kJ·mol-1。试根据表中所列键能数据估算a 的值: (写出 + 或-)。