题目内容
【题目】元素周期表是学习化学的重要工具,它隐含许多信息和规律。
He | |||||||||||||||||
d | e | ||||||||||||||||
a | c | ||||||||||||||||
b | |||||||||||||||||
(1)请在图中用实线补全元素周期表的边界_________________________
(2)写出c在周期表中对应的位置________,并画出其原子结构示意图___________。
(3)相同大小的a、b两种元素的单质分别投入水中,反应较剧烈的是_______(用化学式表示, 下同),其与水反应的化学方程式为_________。
(4)比较d元素和e元素原子半径的大小_________(用“>”连接)。
【答案】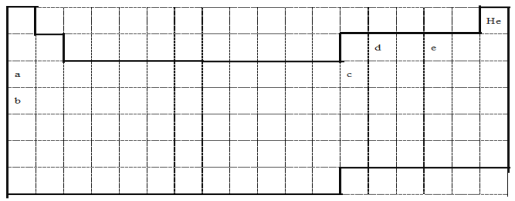 第三周期第ШA族
第三周期第ШA族 ![]() K 2K+H2O=KOH+H2↑ C>O(d>e)
K 2K+H2O=KOH+H2↑ C>O(d>e)
【解析】
(1)根据元素周期表的结构回答;
(2)c是13号元素铝,3个电子层、最外层3个电子。
(3)同主族从上到下金属性增强。
(4)同周期元素从左到右原子半径减小。
(1)元素周期表的边界为
(2)c是13号元素铝,3个电子层、最外层3个电子,在周期表中的位置是第三周期第ШA族;原子结构示意图是![]() 。
。
(3)a、b分别是Na、K,同主族从上到下金属性增强,K的活泼性大于Na,分别投入水中,反应较剧烈的是K。K与水反应生成氢氧化钾和氢气,化学方程式为2K+H2O=KOH+H2↑;
(4)同周期元素从左到右原子半径减小,d是C元素、e是O元素,半径C>O。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目