题目内容
【题目】有X、Y、Z、W、R、Q为前四周期元素,原子序数依次增大。X、Y最外层电子排布可表示为asa,bsbbpb(a≠b),Y、Z、W是位于P区的同一周期的元素,Y与W原子核外的未成对电子数相等,RW2与ZW2-为等电子体,Q为过渡金属元素,其原子核外没有未成对电子。请回答下列问题:
(1)Q的最外层电子排布式为_________ ,RW2的分子立体构型是_________________
(2)Y、Z、W的最简单氢化物中,键角最小的是_______(用分子式表示), YW与Z2互为等电子体,ZW的结构式为____________(若有配位键,请用“→”表示)。
(3)ZX3可以与X+结合成ZX4+,这个过程中发生改变的是____(填序号)。

a.微粒的空间构型 b.Z原子的杂化类型
c.X-Z-X的键角 d.微粒的电子数
(4)QR在荧光体,光导体材料、涂料、颜料等行业中应用广泛。立方QR晶体结构如图所示,一个晶胞中含有的Q原子数为____________。与R原子最近且距离相等的R原子有_____个。该晶胞棱长与最近的两个R原子的距离之比为_______
【答案】 4s2 v形 H2O C≡O ac 4 12 1.4:1
【解析】X、Y、Z、W、R、Q为前四周期元素.X、Y最外层电子排布可表示为asa、bsbbpb(a≠b),Y的最外层电子排布bsbbpb中p轨道有电子,则s轨道一定排满,即b=2,所以Y的最外层电子排布2s22p2,则Y为C元素;s轨道最多排两个电子,已知a≠b,则a=1,所以X的最外层电子排布为1s1,即X为H元素;Y、Z、W是位于P区的同一周期的元素,Y与W原子核外的未成对电子数相等,则W为O元素;RW2与ZW2-为等电子体,可知Z为N元素,R为S元素;Q为过渡金属元素,其原子核外没有未成对电子,则Q为Zn;
(1)Zn的核电荷数为30,其最外层电子排布式为4s2 ,SO2的分子中S原子孤电子对数=![]() =1,价层电子对数=2+1=3,故其空间构型为V形;
=1,价层电子对数=2+1=3,故其空间构型为V形;
(2)CH4为正四面体,H2O为V形,④H3为三角锥形,水分子中含有2对孤对电子,氨气电子中含有1对孤对电子,孤对电子之间排斥作用大于孤对电子与成键电子层之间的排斥作用,所以键角由大到小排列的顺序是CH4>NH3>H2O,键角最小的是H2O;CO与N2互为等电子体,则CO分子中形成三键,且氧原子还提供1对孤对电子与碳原子形成配位键,则CO分子结构式为![]() ,;
,;
(3)NH3分子为三角锥形,键角为107°,NH4+离子为正四面体,键角为109°28′,N原子价层电子对数均为4,均为sp3杂化,核外电子数均为10,则这个过程中发生改变的是微粒的空间构型和A-C-A的键角;
(4)立方ZnS晶体结构如图所示,一个晶胞中含有的Zn原子数为4×1=4;晶胞顶点S原子与晶胞平面中心S原子是距离相等且最近的,则与S原子最近且距离相等的S原子有12个,设最近的两个S原子的距离为acm,则晶胞棱长为![]() acm,晶胞棱长与最近的两个S原子的距离之比为
acm,晶胞棱长与最近的两个S原子的距离之比为![]() :1=1.4:1。
:1=1.4:1。

【题目】亚硝酰氯(ClNO)参与大气平流层和对流层的化学,气相的ClNO光解和水解都可产生Cl自由基。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及的化
学反应、对应的反应热和平衡常数如表:
化学反应 | 反应热 | 平衡常数 |
①2NO2(g)+NaC1(s) | △H1 | K1 |
②2NO(g)+C12(g) | △H2 | K2 |
③4NO2(g)+2NaC1(s) | △H3 | K3 |
则K1,K2,K3之间的关系为K2=______________,△H3=_____________
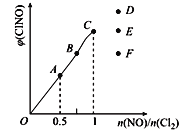
(2)已知2NO(g)+Cl2(g)![]() 2ClNO(g),一定条件下在恒温恒容的密闭容器中按一定比例,充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图,则A、B、C三状态中,NO的转化率最大的是___点,当n(NO)/n(C12)=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的_____点。
2ClNO(g),一定条件下在恒温恒容的密闭容器中按一定比例,充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图,则A、B、C三状态中,NO的转化率最大的是___点,当n(NO)/n(C12)=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的_____点。
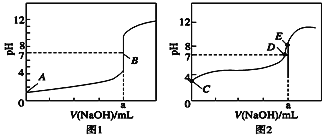
(3)常温下,用0.100 0 mol·L-1 NaOH溶液分别滴定20.00 mL 0.100 0 mol·L-1 HBr溶液和20.00 mL0.100 0 mol·L-1 CH3COOH溶液,得到2条滴定曲线,如图所示:
①根据图1和图2判断,滴定HBr溶液的曲线是______________(填“图1”或“图2”);
②a=______ mL; ③c(Na+)=c(CH3COO-)的点是______点;
④E点对应溶液中离子浓度由大到小的顺序为_______________。
(4) 氨气燃料电池,一极通入氨气,另一极通入空气,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-。写出负极的电极反应式_____________。
(5) 已知:CdCO3、NiCO3溶度积分别为6.0×10-12、1.0×10-7。p(CO32-)=-lg c(CO32-) 。在含Cd2+、Ni2+浓度均为0.01 mol/L的废水中滴加稀碳酸钠溶液。为了分离这两种阳离子,需要控制p(CO32-)范围为_____________(忽略溶液体积的变化)
A.4≤p(CO32-)≤6
B.5<p(CO32-)≤ 7-lg6
C.7-lg6<p(CO32-)≤ 8
D.7<p(CO32-)≤8