题目内容
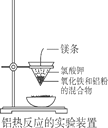
【题目】铝热反应常用来焊接钢轨。下图为实验室进行铝热反应的装置,点燃镁条,反应过程中看到熔融物落入蒸发皿的沙子中。则下列有关说法中正确的是
A. 金属氧化物与铝都能发生铝热反应
B. 该装置所用的漏斗是玻璃漏斗
C. 反应中观察到熔融物落入蒸发皿中,表明该反应是放热反应
D. 加氯酸钾的目的是用氯酸钾来氧化铝粉
【答案】C
【解析】
A、活泼性大于铝的金属的氧化物不能发生铝热反应,如铝和氧化镁不能发生铝热反应,故A错误;
B、铝热反应放出大量的热,该装置所用的漏斗是用滤纸等材料制作的漏斗状的容器,不能使用玻璃仪器,故B错误;
C、反应产物呈熔融状态,说明反应是放热反应,故C正确;
D、氯酸钾受热分解可生成氧气,促进镁条燃烧更旺从而产生高温引发铝热反应,故D错误。

【题目】取一小块金属钠放在燃烧匙中加热,下列实验现象描述正确的是( )
①金属钠先熔化②在空气中燃烧,产生黄色火焰 ③燃烧后得白色固体 ④燃烧后生成淡黄色固体物质
A.①②④B.①②③C.①②D.①②③④
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:

苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴。向a中滴入几滴溴,有白色烟雾产生。请分别写出a仪器和c仪器的名称:_________________________、________________________________。
(2)请写出a中发生反应的化学方程式:___________________。d中倒置漏斗的作用是:_____,某同学认为如果想验证该反应的类型,可以取反应后烧杯d中溶液,加入稀硝酸酸化,然后加入硝酸银溶液,如果产生了淡黄色沉淀即验证了该反应的类型。试分析该同学的操作是否可行:______(填“是”或“否”),简要说明其原因:________________________。
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。
经以上分离操作后,粗溴苯中还含有的主要杂质为___,要进一步提纯,下列操作中必须的是____(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
【题目】元素周期表是学习化学的重要工具,它隐含许多信息和规律。
He | |||||||||||||||||
d | e | ||||||||||||||||
a | c | ||||||||||||||||
b | |||||||||||||||||
(1)请在图中用实线补全元素周期表的边界_________________________
(2)写出c在周期表中对应的位置________,并画出其原子结构示意图___________。
(3)相同大小的a、b两种元素的单质分别投入水中,反应较剧烈的是_______(用化学式表示, 下同),其与水反应的化学方程式为_________。
(4)比较d元素和e元素原子半径的大小_________(用“>”连接)。