题目内容
下列实验操作中正确的是
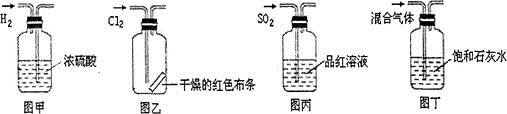

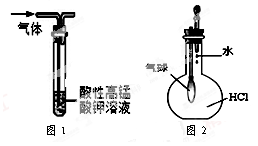
| A.图甲所示,可得到干燥的氢气 |
| B.图乙所示,可以验证氯气的漂白性 |
| C.图丙所示,可以验证SO2的漂白性 |
| D.图丁所示,若石灰水变浑浊,证明混合气体中一定含有CO2 |
D
A中不能得到干燥的氢气,因为进入管短,会把浓硫酸从长导管中压出,A错;布条是干燥的,无漂白性,B错;二氧化硫能使品红溶液褪色,证明二氧化硫的漂白性,C正确;能使澄清石灰水变浑浊不光是二氧化碳,也可能是二氧化硫,D错。答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目




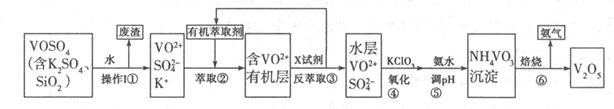
 2RAn(有机层)+nH2SO4(水层),
2RAn(有机层)+nH2SO4(水层),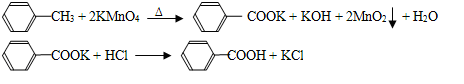
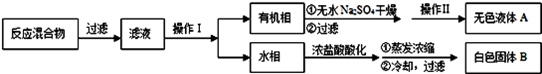
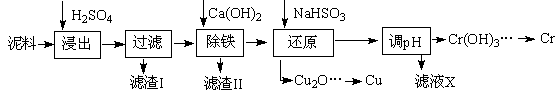
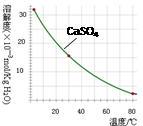
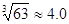 )
)