题目内容
3.下列现象分别是由氯水中的何种粒子引起的,将其化学式填写在短线上A.氯水呈浅黄绿色Cl2
B.向NaOHCO3溶液中滴加氯水.有气泡逸出H+
c.向AgNO3溶液中滴加氯水,有白色沉淀产生Cl-
D.氯水光照后有氧气生成HClO
E.氯水滴入浅绿色的FeCl2溶液中,溶液变成黄色Cl2
F.氯水能使有色布条褪色HClO
G.氯水滴在蓝色石蕊试纸上先变红后褪色H+、HClO
H.用氯水进行消毒和漂白HClO
(5)实验室保存氯水的方法:用化学方程式表示其原因棕色试剂瓶避光保存,2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑.
分析 氯气溶于水发生反应Cl2+H2O?HCl+HClO,新制氯水含有Cl2、H2O、HClO、H+、Cl-等粒子,其中Cl2具有黄绿色,而Cl2、HClO具有强氧化性,HClO具有漂白性,溶液中含有Cl-可与硝酸银反应生成白色AgCl沉淀,其中H+可与碳酸氢钠溶液等物质反应,次氯酸见光易分解,所以氯水要避光保存,以此解答该题.
解答 解:A.氯气的颜色是黄绿色,溶液呈淡黄绿色是含有Cl2;
B.氯水中含有氢离子,能与NaHCO3溶液反应生成二氧化碳气体;
C.溶液中含有Cl-,Cl-可与硝酸银反应生成白色AgCl沉淀;
D.氯水中的次氯酸不稳定光照后会分解生成氧气;
E.氯气具有氧化性,能把亚铁离子氧化为铁离子,则氯水滴入浅绿色的FeCl2溶液中,溶液变成黄色,是因为氯气的氧化性;
F.HClO具有漂白性,可使有色物质褪色;
G.氯水滴在蓝色石蕊试纸上氢离子使其变红色,HClO具有漂白性,使其褪色;
H.HClO具有强氧化性,可以用于消毒和漂白;
故答案为:Cl2;H+;Cl-;HClO;Cl2;HClO;H+、HClO;HClO;
(5)新制氯水中的次氯酸不稳定,见光易分解,次氯酸分解得到盐酸和氧气,2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,所以新制的氯水保存方法为:棕色试剂瓶避光保存,
故答案为:棕色试剂瓶避光保存;2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑.
点评 本题综合考查氯气和氯水的性质,注意把握氯气和水反应的特点以及氯水的成分和性质,为高考高频考点,侧重于基础知识的综合运用,难度不大.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
13.下列化学反应的离子方程式正确的是( )
| A. | 碳酸钙与盐酸溶液反应:2H++CO32-=H2O+CO2 | |
| B. | 铁钉放入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 碳酸氢钠与稀盐酸反应:HCO3-+H+=CO2↑+H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-=BaSO4↓+H2O |
14.食盐、纯碱(Na2CO3)、食醋均为厨房中常用的物质,利用这些物质不能实现的实验是( )
①除去热水瓶内壁的水垢(CaCO3) ②检验自来水中是否含有氯离子
③检验镁粉中是否含有锌粉 ④鉴别食盐和纯碱(Na2CO3)
①除去热水瓶内壁的水垢(CaCO3) ②检验自来水中是否含有氯离子
③检验镁粉中是否含有锌粉 ④鉴别食盐和纯碱(Na2CO3)
| A. | ①④ | B. | ②③ | C. | ②④ | D. | ①② |
5.下列关于钠与水反应的说法不正确的是( )
①将小块钠投入滴有石蕊试液的水中,反应后溶液变红
②将钠投入稀盐酸中,钠先与水反应,后与盐酸反应
③钠在水蒸气中反应时因温度高会燃烧
④钠与氧气反应的产物为过氧化钠.
①将小块钠投入滴有石蕊试液的水中,反应后溶液变红
②将钠投入稀盐酸中,钠先与水反应,后与盐酸反应
③钠在水蒸气中反应时因温度高会燃烧
④钠与氧气反应的产物为过氧化钠.
| A. | 只有①② | B. | 只有②③ | C. | 只有②③④ | D. | ①②③④ |
6.硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、漂白粉等一系列物质(见如图).下列说法正确的是
( )

( )

| A. | CO、SO2、SO3均是酸性氧化物 | |
| B. | 工业上利用Cl2和澄清石灰水反应来制取漂白粉 | |
| C. | 漂白粉的有效成分为Ca(ClO)2 | |
| D. | 除去与水反应的两个反应,图示其余转化反应均为氧化还原反应 |
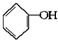 合成
合成 (部分试剂和反应条件已略去).
(部分试剂和反应条件已略去).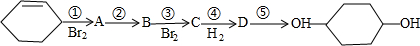
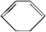 、D
、D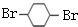 .
.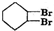 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ .
.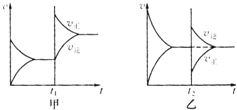 在一定条件下,有反应xA+yB?zC.
在一定条件下,有反应xA+yB?zC.