题目内容
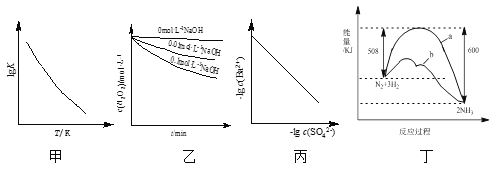
【题目】如右图所示,把试管放入盛有25 ℃饱和澄清石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入10 mL盐酸于试管中,试回答下列问题:
(1)实验中观察到的现象是________________________________ 。
(2)产生上述现象的原因是____________________________。
(3)写出有关反应的离子方程式:_________________________________;
反应中转移了0. 04mol电子时;标准状况下产生多少________mL的H2;消耗镁多少________g(保留两位小数);生成的MgCl2物质的量浓度为________。(溶液体积保持不变)
(4)由实验推知,镁片溶液和盐酸的总能量________(填“大于”、“小于”或“等于”) MgCl2和H2的总能量;此反应为________ (填放热反应或者吸热反应)。
【答案】镁片上有大量气泡产生,镁片逐渐溶解,烧杯中溶液变浑浊 镁与盐酸反应产生氢气,该反应为放热反应,Ca(OH)2在水中的溶解度随温度升高而减小,故析出Ca(OH)2晶体 Mg+2H+=Mg2++H2↑ 448 0.48 2.0mol/L 大于 放热反应
【解析】
(1)、(2)镁是活泼金属,能与稀盐酸发生反应,在镁片上产生大量气泡,即产生氢气,随着反应的进行,镁片逐渐溶解,该反应放出大量的热,而饱和石灰水随着温度的升高,溶解度逐渐减小,逐渐有Ca(OH)2晶析析出,所以烧杯中溶液变浑浊;
(3)该反应的离子的方程式为Mg+2H+=Mg2++H2↑;反应中转移了0. 04mol电子时,即生成0.02molH2,标准状况下产生448mL的H2;消耗镁0.02molMg,即消耗镁:![]() ;生成的MgCl2物质的量浓度为
;生成的MgCl2物质的量浓度为![]() ;
;
(4)由实验可知,该反应为放热反应,反应物的总能量大于生成物的总能量,所以镁片溶液和盐酸的总能量大于MgCl2和H2的总能量。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】已知:下表为25℃时某些弱酸的电离平衡常数。
CH3COOH | HClO | H2CO3 |
Ka=1.8×10﹣5 | Ka=3.0×10﹣8 | Ka1=4.4×10﹣7Ka2=4.7×10﹣11 |
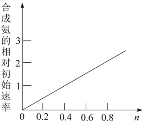
如图表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( )

A.Ⅰ曲线代表HClO,Ⅱ曲线代表CH3COOH
B.向NaClO溶液中通入少量二氧化碳的离子方程式为:ClO﹣+CO2+H2O=HClO+CO32-
C.图象中a、c两点处的溶液中![]() 相等(HR代表CH3COOH或HClO)
相等(HR代表CH3COOH或HClO)
D.图象中a点酸的总浓度大于b点酸的总浓度