题目内容
下列各组离子因发生氧化还原反应而不能大量共存的是( )
A.pH=1的溶液中:Fe2+、Al3+、K+、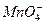 |
B.某无色溶液中:K+、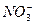 、Cl-、 、Cl-、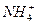 |
C.含有大量OH-的溶液中:Na+、Cu2+、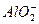 、 、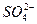 |
D.常温下由水电离出的c(H+)=10-10 mol·L-1的溶液中:Na+、Cl-、F-、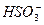 |
A
A项Fe2+与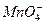 发生氧化还原反应,不能大量共存;B项中各离子可以大量共存;C项中的OH-与Cu2+因发生复分解反应,而不能大量共存;D项,溶液可以是酸性的,也可以是碱性的,如果是酸性的,H+与F-、
发生氧化还原反应,不能大量共存;B项中各离子可以大量共存;C项中的OH-与Cu2+因发生复分解反应,而不能大量共存;D项,溶液可以是酸性的,也可以是碱性的,如果是酸性的,H+与F-、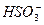 发生复分解反应,如果是碱性的,OH-与
发生复分解反应,如果是碱性的,OH-与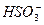 发生复分解反应,所以不论溶液显酸性还是显碱性,离子都不能大量共存。
发生复分解反应,所以不论溶液显酸性还是显碱性,离子都不能大量共存。
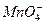 发生氧化还原反应,不能大量共存;B项中各离子可以大量共存;C项中的OH-与Cu2+因发生复分解反应,而不能大量共存;D项,溶液可以是酸性的,也可以是碱性的,如果是酸性的,H+与F-、
发生氧化还原反应,不能大量共存;B项中各离子可以大量共存;C项中的OH-与Cu2+因发生复分解反应,而不能大量共存;D项,溶液可以是酸性的,也可以是碱性的,如果是酸性的,H+与F-、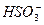 发生复分解反应,如果是碱性的,OH-与
发生复分解反应,如果是碱性的,OH-与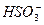 发生复分解反应,所以不论溶液显酸性还是显碱性,离子都不能大量共存。
发生复分解反应,所以不论溶液显酸性还是显碱性,离子都不能大量共存。
练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目