题目内容
(1)在新生代的海水里有一种铁细菌,它们摄取海水中的亚铁离子,把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿;用酶作催化剂时反应的另一个反应物是CO2,它在反应后转变成有机物,可用甲醛来表示,试写出离子方程式,并配平为_____________________;
(2)地球化学家用实验证实,金矿常与磁铁矿共生的原因是:在高温高压的水溶液(即所谓“热液”)里,金的存在形式是[AuS]-络离子,在溶液接近中性时,它遇到Fe2+会发生反应,同时沉淀出磁铁矿和金矿,试写出离子方程式,并配平为___________________________。
(2)地球化学家用实验证实,金矿常与磁铁矿共生的原因是:在高温高压的水溶液(即所谓“热液”)里,金的存在形式是[AuS]-络离子,在溶液接近中性时,它遇到Fe2+会发生反应,同时沉淀出磁铁矿和金矿,试写出离子方程式,并配平为___________________________。
(1)4Fe2++CO2+5H2O====2Fe2O3+HCHO+8H+
(2)2[AuS]-+3Fe2++4H2O====Fe3O4+2Au+2H2S↑+4H+
(2)2[AuS]-+3Fe2++4H2O====Fe3O4+2Au+2H2S↑+4H+
(1)由题意可知反应物是Fe2+和CO2,其中还原剂是Fe2+,方程式为4Fe2++CO2+5H2O====2Fe2O3+HCHO+8H+;
(2)[AuS]-中的Au(+1价)为氧化剂,反应的离子方程式为:2[AuS]-+3Fe2++4H2O====Fe3O4+2Au+H2S↑+4H+。
(2)[AuS]-中的Au(+1价)为氧化剂,反应的离子方程式为:2[AuS]-+3Fe2++4H2O====Fe3O4+2Au+H2S↑+4H+。

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
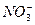 。则该溶液中可能存在的离子组是( )
。则该溶液中可能存在的离子组是( )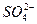 、
、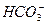 、Cl-、K+
、Cl-、K+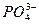 、Zn2+
、Zn2+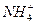 、Mg2+、Cl-、K+
、Mg2+、Cl-、K+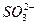 、Na+、Cl-、OH-
、Na+、Cl-、OH-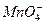
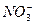 、Cl-、
、Cl-、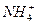
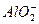 、
、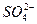
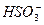

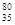 Br
Br