题目内容
【题目】某研究性学习小组进行如下探究活动:
实验目的:探究Cl2、Br2、I2的氧化性强弱。
查阅资料:①常温下,高锰酸钾与浓盐酸反应产生氯气;②溴单质易挥发,碘单质易升华;③淀粉溶液遇到碘单质变蓝色;④溴、碘在不同溶剂中所形成溶液(从稀到浓)的颜色变化如图所示。
水 | 四氯化碳 | |
溴 | 黄→棕 | 橙→橙红 |
碘 | 深黄→褐 | 紫→深紫 |
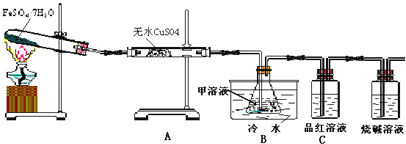
实验方案:该小组设计下图所示装置实验(夹持仪器已略去,装置气密性完好)

实验过程:
Ⅰ 先打开弹簧夹,再打开活塞a,滴加浓盐酸
Ⅱ 当B和C中的溶液都变黄时,加紧弹簧夹
Ⅲ 当B中的溶液由黄色变为棕色时,关闭活塞a
Ⅳ … …
回答以下问题:
(1)验证氯气的氧化性强于碘的实验现象是____________________________,写出该反应的化学方程式__________________________________;
(2)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是_____________________,写出该反应的离子方程式_______________________;
(3)由实验得到的氯、溴、碘单质的氧化性由强到弱的顺序为____________;
(4)你认为实验中为什么要加过程Ⅲ这一步操作,请简述个人观点______________
【答案】A中湿润的淀粉碘化钾试纸变蓝 Cl2+2KI═I2+2KCl 打开活塞b,将分液漏斗中的黄色溶液滴入D中,关闭活塞b,取下试管D振荡,静置,观察到D中CCl4层溶液变为紫红色,说明溴的氧化性强于碘 2I﹣+Br 2=2Br﹣+I2 Cl2>Br2>I2 B、C中的NaBr溶液的浓度和体积均相同,棕色溶液B含有的溴单质比黄色溶液C中的多,说明C中还存有溴离子,不存在氯气,确保了氯气不干扰溴与碘化钾的反应
【解析】
(1)装置①中可以生成氯气,氯气具有强氧化性,能把碘化钾氧化生成单质碘,碘遇淀粉显蓝色,所以验证氯气的氧化性强于碘的实验现象是A中湿润的淀粉碘化钾试纸变蓝;反应的化学方程式是2KI+Cl2=2KCl+I2;
(2)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是打开活塞b,将分液漏斗中的黄色溶液滴入D中,关闭活塞b,取下试管D振荡、静置,观察到D中四氯化碳层呈紫色,说明溴的氧化性强于碘;该反应的离子方程式为Br2+2I-=2Br-+I2;
(3)根据上述两个实验,对同一个化学反应而言,氧化剂的氧化性大于氧化产物的氧化性,则Cl2>Br2,Br2>I2,所以氯、溴、碘单质的氧化性由强到弱的顺序为Cl2、Br2、I2;
(4)B、C中的NaBr溶液的浓度和体积均相同,棕色溶液B含有的溴单质比黄色溶液C中的多,说明C中还存有溴离子,不存在氯气,确保了氯气不干扰溴与碘化钾的反应,所以实验中要加过程Ⅲ这一步操作。