题目内容
【题目】
金属铁及其化合物在材料、航空工业上有重要用途。回答下列相关问题:
(1)基态钛原子中有__________个状态不同的电子,最高能层电子的电子云轮廓图形状为__________,写出其价电子的轨道表达式__________。
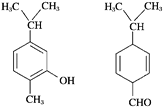
(2)化合物TiO2不仅是常用的白色颜料,也是一些反应的良好催化剂,如:

有机物X中C原子的杂化轨道类型为__________,1mol Y中所含σ键的数目是__________。
(3)已知TiCl4在常温下是无色液体,TiCl4的晶体类型是__________晶体,其空间构型是__________。
(4)自然界中有丰富的钛矿资源,如右图表示的是钡钛矿晶体的晶胞结构,经X射线分析,该晶胞为正方体,晶胞参数为apm。
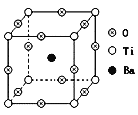
写出钡钛矿晶体的化学式__________,其密度是__________g·cm-3。
【答案】22 球形 ![]() sp3、sp2 16NA 分子 正四面体 BaTiO3 233/(a×10-10)3·NA
sp3、sp2 16NA 分子 正四面体 BaTiO3 233/(a×10-10)3·NA
【解析】
(1)钛原子的核电荷数为22,其核外共有22个运动状态不同的电子,钛原子的价电子排布式为3d24s2,则价电子排布图为![]() ,最高能层电子的电子云轮廓图形状为球形,;故答案为:22;球形;
,最高能层电子的电子云轮廓图形状为球形,;故答案为:22;球形; ![]() ;
;
(2)有机物X(![]() )中C原子有2种类型,其中甲基进而亚甲基中的碳原子均采用sp3杂化,羰基中的碳原子采用sp2杂化,单键是1个σ键,双键是1个σ键和1个π键,1molY(
)中C原子有2种类型,其中甲基进而亚甲基中的碳原子均采用sp3杂化,羰基中的碳原子采用sp2杂化,单键是1个σ键,双键是1个σ键和1个π键,1molY(![]() )中所含σ键的数目是16NA,故答案为:sp3、sp2;16NA;
)中所含σ键的数目是16NA,故答案为:sp3、sp2;16NA;
(3)已知TiCl4在常温下是无色液体,说明其熔沸点较低,则TiCl4属于分子晶体,其中Ti采用sp3杂化,空间构型为正四面体,故答案为:分子晶体;正四面体;
(4)由结构可知,Ba位于体心有1个,Ti位于顶点,数目为8×![]() =1个,O位于棱心,数目为12×
=1个,O位于棱心,数目为12×![]() =3个,故其化学式为BaTiO3;在每个晶胞中含有一个BaTiO3,质量为
=3个,故其化学式为BaTiO3;在每个晶胞中含有一个BaTiO3,质量为![]() g;晶体密度ρ=
g;晶体密度ρ=![]() =
=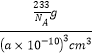 =
=![]() g/cm3,故答案为:BaTiO3;
g/cm3,故答案为:BaTiO3;![]() 。
。