题目内容
【题目】分析下图所示的四个原电池装置,其中结论正确的是
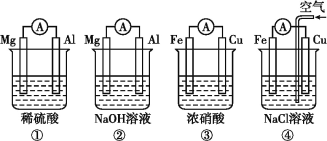
A. ①②中Mg作负极,③④中Fe作负极
B. ②中Mg作正极,电极反应式为6H2O+6e6OH+3H2↑
C. ③中Fe作负极,电极反应式为Fe3eFe3+
D. ④中Cu作正极,电极反应式为2H++2eH2↑
【答案】B
【解析】
A.②中Mg不与NaOH溶液反应,而Al能和NaOH溶液反应失去电子,故Al是负极;③中Fe在浓硝酸中钝化,Cu和浓硝酸反应失去电子作负极,故A不正确;
B.②中电池总反应为2Al+2NaOH+2H2O2NaAlO2+3H2↑,负极反应式为2Al+8OH6e2![]() +4H2O,两者相减得到正极反应式为6H2O+6e6OH+3H2↑,故B正确;
+4H2O,两者相减得到正极反应式为6H2O+6e6OH+3H2↑,故B正确;
C.③中Fe在浓硝酸中钝化,Cu和浓硝酸反应失去电子作负极,故C不正确;
D.④中Cu是正极,电极反应式为O2+2H2O+4e4OH,故D不正确;
正确答案:B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】下列用来解释实验事实的相关平衡方程式不正确的是
实验事实 | 相关平衡 | |
A | 加入NaHCO3使氯水的漂白能力增强 | Cl2+H2O |
B | 配制FeCl3溶液时加少量盐酸 | Fe3++3OH- |
C | 溶有CO2的正常雨水pH≈5.6 | H2O+CO2 |
D | CaCO3固体溶于盐酸 | CaCO3(s) |
A. A B. B C. C D. D