题目内容
17.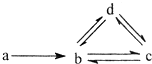 下列各组物质依次满足如图所示转化关系的是(图中箭头表示一步转化)( )
下列各组物质依次满足如图所示转化关系的是(图中箭头表示一步转化)( )| a | b | c | d | |
| ① | Si | SiO2 | H2SiO3 | Na2SiO3 |
| ② | N2 | NO | NO2 | HNO3 |
| ③ | Cu | CuO | Cu(OH)2 | CuSO4 |
| ④ | Na | NaCl | Na2CO3 | NaHCO3 |
| A. | ①② | B. | ②③ | C. | ③④ | D. | ② |
分析 ①二氧化硅与水不反应;
②氮气与氧气反应生成一氧化氮,一氧化氮氧化生成二氧化氮,二氧化氮与水反应生成硝酸,稀硝酸与铜反应生成一氧化氮;
③氧化铜不溶于水;
④盐酸酸性强于碳酸,不能一步实现氯化钠到碳酸钠的转化.
解答 解:①二氧化硅与水不反应,b→c不能实现,故错误;
②氮气与氧气反应生成一氧化氮,一氧化氮氧化生成二氧化氮,二氧化氮与水反应生成硝酸,稀硝酸与铜反应生成一氧化氮,符合上述转化关系,故正确;
③氧化铜不溶于水,与水不反应b→c不能实现,故错误;
④盐酸酸性强于碳酸,不能一步实现氯化钠到碳酸钠的转化,故错误;
故选:D.
点评 本题考查了物质之间的转化,熟悉物质的性质是解题关键,侧重考查学生对常见物质性质的考查,题目难度不大.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
8.化学在物质制备和环保领域有着重要的运用.
Ⅰ高铁酸盐在能源、环保等方面有着广泛的用途.湿法、干法制备高铁酸盐的原理如下表所示.
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如图1所示:
①反应I的化学方程式为2NaOH+Cl2═NaCl+NaClO+H2O.
②反应II的离子方程式为3ClO-+10OH-+2Fe3+=2FeO42-+3Cl-+5H2O.
③已知25℃时Fe(OH)3的Ksp=4.0×10-38,反应II后溶液中c(Fe3+)=4×10-5mol•L-1,则Fe3+完全沉淀时的pH=3.
(2)高铁酸钾是一种理想的水处理剂,其处理水的原理为高铁酸钾有强氧化性,能杀菌消毒,在水中被还原生成Fe(OH)3胶体、有吸附性起净水作用.
(3)干法制备K2FeO4的反应中氧化剂与还原剂的物质的量之比为3﹕1.
(4)高铁电池是正在研制中的可充电干电池,图2为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有放电时间长、工作电压稳定.

Ⅰ高铁酸盐在能源、环保等方面有着广泛的用途.湿法、干法制备高铁酸盐的原理如下表所示.
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
①反应I的化学方程式为2NaOH+Cl2═NaCl+NaClO+H2O.
②反应II的离子方程式为3ClO-+10OH-+2Fe3+=2FeO42-+3Cl-+5H2O.
③已知25℃时Fe(OH)3的Ksp=4.0×10-38,反应II后溶液中c(Fe3+)=4×10-5mol•L-1,则Fe3+完全沉淀时的pH=3.
(2)高铁酸钾是一种理想的水处理剂,其处理水的原理为高铁酸钾有强氧化性,能杀菌消毒,在水中被还原生成Fe(OH)3胶体、有吸附性起净水作用.
(3)干法制备K2FeO4的反应中氧化剂与还原剂的物质的量之比为3﹕1.
(4)高铁电池是正在研制中的可充电干电池,图2为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有放电时间长、工作电压稳定.

2.下列化学用语的表述对应正确的是( )
| A. | 碳酸氢钠的电离方程式:NaHCO3═Na++H++CO${\;}_{3}^{2-}$ | |
| B. | 用铜做阳极电解氯化铜溶液的离子方程式:Cu2++2Cl-$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑ | |
| C. | 硫化钠水解的离子方程式:S2-+2H2O═H2S+2OH- | |
| D. | 用TiCl4制备TiO2的化学方程式:TiCl4+(x+2)H2O(过量)?TiO2•x H2O↓+4HCl |
7.下列关于物质的量的说法正确的是( )
| A. | 摩尔是国际单位制中7个基本物理量之一 | |
| B. | 物质的量就是物质的质量 | |
| C. | 物质的量像一座桥梁,把物质的质量或体积等宏观量与微观粒子的数量联系起来 | |
| D. | 是表示物质数量的单位 |

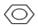 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr.
+HBr. 过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用.
过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用.
