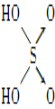题目内容
【题目】下列反应的离子方程式书写不正确的是( )
A.钠与水反应:Na+H2O=Na++OH-+H2↑
B.氯化钡溶液与稀硫酸反应:Ba2++SO![]() =BaSO4↓
=BaSO4↓
C.碳酸钠溶液与足量盐酸反应:CO![]() +2H+=CO2↑+H2O
+2H+=CO2↑+H2O
D.铜与稀硝酸反应:3Cu+8H++2NO![]() =3Cu2++2NO↑+4H2O
=3Cu2++2NO↑+4H2O
【答案】A
【解析】
A.钠与水反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑,题中原子不守恒,A选项错误;
B.氯化钡溶液与稀硫酸反应生成硫酸钡的沉淀和HCl,离子方程式为Ba2++SO![]() =BaSO4↓,B选项正确;
=BaSO4↓,B选项正确;
C.碳酸钠溶液与足量盐酸反应生成NaCl、CO2和H2O,离子方程式为CO![]() +2H+=CO2↑+H2O,C选项正确;
+2H+=CO2↑+H2O,C选项正确;
D.铜与稀硝酸反应生成Cu(NO3)2、NO和H2O,离子方程式为3Cu+8H++2NO![]() =3Cu2++2NO↑+4H2O,D选项正确;
=3Cu2++2NO↑+4H2O,D选项正确;
答案选A。

【题目】[化学-选修2:化学与技术]
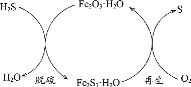
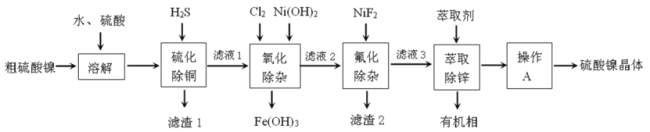
双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程如图所示:


A.氢化釜 | B.过滤器 | C.氧化塔 | D.萃取塔E.净化塔F.工作液再生装置G.工作液配制装置 |
生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定的温度、压力和催化剂作用下进行氢化,再经氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备双氧水理论上消耗的原料是_______,循环使用的|原料是______,配制工作液时采用有机溶剂而不采用水的原因是______。
(2)氢化釜A中反应的化学方程式为_______,进入氧化塔C的反应混合液中的主要溶质为_______。
(3)萃取塔D中的萃取剂是____,选择其作萃取剂的原因是______。
(4)工作液再生装置F中要除净残留的H2O2,原因是______。
(5)双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为_______。一种双氧水的质量分数为27.5%,(密度为1.10g·cm3),其浓度为______mol/L。
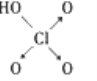
【题目】判断含氧酸酸性强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。如下表所示:
含氧酸酸性强弱与非羟基氧原子数的关系
次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
含氧酸 | Cl—OH |
|
|
|
非羟基氧原子数 | 0 | 1 | 2 | 3 |
酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
(1)已知,亚磷酸是中强酸,亚砷酸是弱酸且有一定的弱碱性,则H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是①_____________________________,②__________________________________。
(2)在H3PO3和H3AsO3中分别加入浓盐酸,分析反应情况______________,写出化学方程式:____________________________________________________。