题目内容
已知:S(s)+O2(g)→SO2(g) +297.16kJ,2SO2(g)+O2(g) 2SO3(g)+196.6 kJ,下列说法正确的是
2SO3(g)+196.6 kJ,下列说法正确的是
 2SO3(g)+196.6 kJ,下列说法正确的是
2SO3(g)+196.6 kJ,下列说法正确的是| A.1 molSO2(g)的能量总和大于lmol S(s)和l molO2(g)的能量总和 |
| B.将2 molSO2(g)与l molO2(g)在一定条件下充分反应,放出196.6kJ的热量 |
C.S(g)+O2(g) SO2(g)+Q,Q值小于297.16 kJ SO2(g)+Q,Q值小于297.16 kJ |
| D.当l mol S(s)完全转化为SO3(g)时(假设无热量损失),放出395.46kJ的热量 |
D
试题分析:A、S燃烧生成SO2的反应是放热反应,所以1 molSO2(g)的能量总和小于lmol S(s)和l molO2(g)的能量总和,A不正确;B、反应2SO2(g)+O2(g)
 2SO3(g) 是可逆反应,反应物的转化率得不到100%,因此将2 molSO2(g)与l molO2(g)在一定条件下充分反应,放出的热量小于196.6kJ,B不正确;C、气态S的能量高于固态S的能量,所以气态S燃烧放出的热量多,即S(g)+O2(g)→SO2(g)+Q,Q值大于297.16 kJ,C不正确;D、根据盖斯定律可知,S(s)+
2SO3(g) 是可逆反应,反应物的转化率得不到100%,因此将2 molSO2(g)与l molO2(g)在一定条件下充分反应,放出的热量小于196.6kJ,B不正确;C、气态S的能量高于固态S的能量,所以气态S燃烧放出的热量多,即S(g)+O2(g)→SO2(g)+Q,Q值大于297.16 kJ,C不正确;D、根据盖斯定律可知,S(s)+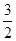 O2(g)→SO3(g),所以该反应放出的热量是297.16kJ+
O2(g)→SO3(g),所以该反应放出的热量是297.16kJ+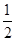 ×196.6 kJ=395.46kJ,D正确,答案选D。
×196.6 kJ=395.46kJ,D正确,答案选D。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 3N2+2X+4H2O
3N2+2X+4H2O  .
. 、一283.0 kJ
、一283.0 kJ 、
、 均大于300℃):
均大于300℃):
 时,从反应开始到反应达到平衡,生成甲醇的平均速率为:
时,从反应开始到反应达到平衡,生成甲醇的平均速率为:
 增大
增大 4NO(g)+6H2O(g) △H =" —905" kJ/mol ①主反应
4NO(g)+6H2O(g) △H =" —905" kJ/mol ①主反应
 N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T。C)条件下反应,反应进行到不同时间测得各物质的浓度如下
N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T。C)条件下反应,反应进行到不同时间测得各物质的浓度如下
 N2+2CO2 ΔH<0研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.为了分别验证温度、催化剂的比表面积对化学反 应速率的影响规律、某同学设计了三组实验,部分实验条件已经填在下表中。
N2+2CO2 ΔH<0研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.为了分别验证温度、催化剂的比表面积对化学反 应速率的影响规律、某同学设计了三组实验,部分实验条件已经填在下表中。


 H2O(l) 的ΔH ="+" 40.69 kJ·mol-1
H2O(l) 的ΔH ="+" 40.69 kJ·mol-1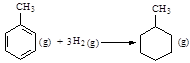 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1 2SO3(g) △H="-Q" kJ·mol-1(Q>0),测得SO2的转化率为90%,
2SO3(g) △H="-Q" kJ·mol-1(Q>0),测得SO2的转化率为90%,