题目内容
下列关于各图的叙述中,正确的是

A.图甲表示1mol H2 (g)完全燃烧生成水蒸气吸收241.8 kJ热量
B.图甲表示2 mol H2(g)所具有的能量比2 molH2O(g)所具有的能量多483.6 kJ
C.图乙表示常温下稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同温、同浓度的NaA溶液的pH小于NaB溶液的pH
D.图乙中起始时HA的物质的量浓度大于HB

A.图甲表示1mol H2 (g)完全燃烧生成水蒸气吸收241.8 kJ热量
B.图甲表示2 mol H2(g)所具有的能量比2 molH2O(g)所具有的能量多483.6 kJ
C.图乙表示常温下稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同温、同浓度的NaA溶液的pH小于NaB溶液的pH
D.图乙中起始时HA的物质的量浓度大于HB
C
试题分析:A、图甲中反应物的总能量高于生成物的总能量,反应是放热反应,因此表示1mol H2 (g)完全燃烧生成水蒸气放出483.6kJ÷2=241.8 kJ热量,A不正确;B、图甲表示2mol H2(g)和1mol氧气所具有的能量比2molH2O(g)所具有的能量多483.6 kJ,B不正确;C、根据图乙可知,在稀释过程中HA的pH变化程度大于HB的变化程度,所以HA的酸性大于HB的酸性。酸越弱,相应的钠盐越容易水解,所以同温、同浓度的NaA溶液的pH小于NaB溶液的pH,C正确;D、HA的酸性大于HB的酸性,所以图乙中起始时HA的物质的量浓度小于HB,D不正确,答案选C。

练习册系列答案
相关题目
 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol 键、H—H键键分别需吸收的能量为946 kJ、436 kJ,则断开1molN—H需吸收的能量为 kJ。
键、H—H键键分别需吸收的能量为946 kJ、436 kJ,则断开1molN—H需吸收的能量为 kJ。

 2SO3(g)+196.6 kJ,下列说法正确的是
2SO3(g)+196.6 kJ,下列说法正确的是 SO2(g)+Q,Q值小于297.16 kJ
SO2(g)+Q,Q值小于297.16 kJ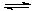 H++ SO42-
H++ SO42- 的废水会发生如下反应:
的废水会发生如下反应:
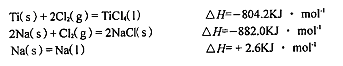
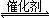 2CO2(g)+S(l) △H
2CO2(g)+S(l) △H
 HSO3—的平衡常数K="8.0" × 106 L?mol-1,计算时SO2、H2SO3的浓度忽略不计)
HSO3—的平衡常数K="8.0" × 106 L?mol-1,计算时SO2、H2SO3的浓度忽略不计)