��Ŀ����
��10�֣�Ϊ�˲ⶨ���ᾧ�壨H2C2O4��xH2O���е�xֵ����������ʵ��
��1����ȡWg���ᾧ�壬���100.00mL��Һ
��2��ȡ25.00mL������Һ����ƿ�ڣ���������ϡH2SO4����Ũ��Ϊamol/L��KMnO4��Һ�ζ���KMnO4������ɫΪֹ���������ķ�ӦΪ�� 2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2��+2MnSO4+8H2O��
�Իش�
��ʵ���У���Ҫ�������У�����ţ� ����ȱ�ٵ������У������ƣ�
A������ƽ�������롢���ӣ� B�ζ��� C 100mL����Ͳ D��100mL������ƿ
E���ձ� F��©�� G����ƿ H�������� I��ҩ�� J����ƿ
��ʵ���У���KMnO4��ҺӦװ�� ʽ�ζ����У���Ϊ
�����ڽӽ��ζ��յ�ʱ������������ˮ����ƿ�ڱڳ�ϴһ�£��ټ��������յ㣬������õ�x��ֵ�� ����ƫ��ƫС����Ӱ�죩��
���ڵζ�����������ȥamol/L��KMnO4��ҺVmL���������ƵIJ�����Һ�����ʵ���Ũ��Ϊ mol/L���ɴˣ�x= ��
�����ζ��յ����ʱ���ӿ̶ȣ�������xֵ�� ����ƫ��ƫС����Ӱ�죩��
��A��B��D��E��G��H��I ����ͷ�ιܡ�����̨���ζ��ܼ� ��
���� ��KMnO4��Һ�и�ʴ�ԣ��ḯʴ������Ӱ��
��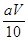 �� x=
�� x=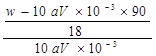 ����
����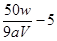 ���� ƫ�� ��
���� ƫ�� ��
��������������ٸ���������Һ��Ҫ��������֪���ڸ�ʵ���У���Ҫ��������A��B��D��E��G��H��I ����ȱ�ٵ������н�ͷ�ιܡ�����̨���ζ��ܼУ���ʵ���У���KMnO4��Һ��Ϊ��ǿ�����ԣ��ḯʴ�ܣ�����Ӧ��Ӧװ����ʽ�ζ����У������ڽӽ��ζ��յ�ʱ������������ˮ����ƿ�ڱڳ�ϴһ�£��ټ��������յ㣬��Ϊ��ƿ�����ʵ������ȶ�û�б仯������������õ�x��ֵ�����κ�Ӱ�죻�ܸ��ݷ�Ӧ����ʽ2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2��+2MnSO4+8H2O��֪��n(H2C2O4)= 5/2n(KMnO4) ��n(KMnO4)= aV��10-3mol��0.025L��c(H2C2O4)= 5/2��aV��10-3�����c(H2C2O4)=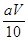 mol/L����[Wg��(90+18x)g/mol]��4=
mol/L����[Wg��(90+18x)g/mol]��4=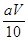 ��0.025mol,���x=
��0.025mol,���x=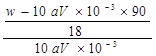 ����
����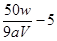 �������ζ��յ����ʱ���ӿ̶ȣ����������ʵ���ƫ�٣������xֵ��ƫ��
�������ζ��յ����ʱ���ӿ̶ȣ����������ʵ���ƫ�٣������xֵ��ƫ��
���㣺�������ʵ���Ũ�ȵ���Һ�����ơ��ζ����ڲⶨ���ʵ�Ũ�Ȼ���������е�Ӧ�õ�֪ʶ��

������ܱ�װ���У��������ƣ�NaClO2��������һ�������·����ֽⷴӦ���������γɵIJ�����
| A��NaCl��O2 | B��NaClO3��NaClO | C��NaClO3��Cl2 | D��NaClO3��NaCl |
��ijFeBr2��Һ�У�ͨ��1.12L����״������Cl2�������Һ��c(Br-)=3c(Cl-)=0.3mol/L����Ӧ��������Һ������仯���ơ�������˵������ȷ����
| A��ԭ��Һ��Ũ��Ϊ0.1mol/L |
| B����Ӧ����Һ��c(Fe3+)=0.1mol/L |
| C����Ӧ����Һ��c(Fe3+)=c(Fe2+) |
| D��ԭ��Һ��c��Br-��=0.4mol/L |
�Ӻ�ˮ�п�����ȡ�壬��Ҫ��ӦΪ��2Br����Cl2===2Cl����Br2������˵����ȷ����(����)
| A�������Ӿ��������� | B�������ǻ�ԭ�� |
| C���÷�Ӧ���ڸ��ֽⷴӦ | D�������������Ա��嵥��ǿ |

 ��ԭΪN2��25��ʱ����Ӧ����10 min����Һ��pH��7��Ϊ12�������£���
��ԭΪN2��25��ʱ����Ӧ����10 min����Һ��pH��7��Ϊ12�������£���