题目内容
Grignard试剂(卤代烃基镁)广泛运用于有机合成中,Grignard试剂的合成方法是:RX+Mg
RMgX(Grignard试剂).生成的卤代烃基镁与具有羰基结构的化合物(醛、酮等)发生反应,再水解就能合成各种指定结构的醇:

现以2-丁烯和必要的无机物为原料合成3,4-二甲基-3-己醇,进而合成一种分子式为C10H16O4的具有六元环的物质J,该物质具有对称性.合成线路如下:
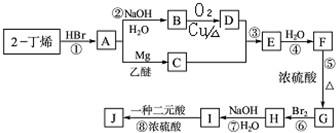
请按要求填空:
(1)用系统命名法对物质B进行命名: ;
(2)在I-J过程中所加入的二元酸的结构简式为: ;
(3)反应①~⑧中属于取代反应的有 个;属于消去反应的有 个.
A.1个 B.2个 C.3个 D.4个
(4)写出下列过程的反应方程式(有机物请用结构简式表示):
B→D ;
I→J ;
(5)写出一种满足以下条件的D的同分异构体的结构简式 .
①能与Na反应反出H2;②核磁共振氢谱有四组峰;③有二种官能团.(注:羟基不能与碳碳双键中的碳原子直接相连)
| 乙醇 |

现以2-丁烯和必要的无机物为原料合成3,4-二甲基-3-己醇,进而合成一种分子式为C10H16O4的具有六元环的物质J,该物质具有对称性.合成线路如下:

请按要求填空:
(1)用系统命名法对物质B进行命名:
(2)在I-J过程中所加入的二元酸的结构简式为:
(3)反应①~⑧中属于取代反应的有
A.1个 B.2个 C.3个 D.4个
(4)写出下列过程的反应方程式(有机物请用结构简式表示):
B→D
I→J
(5)写出一种满足以下条件的D的同分异构体的结构简式
①能与Na反应反出H2;②核磁共振氢谱有四组峰;③有二种官能团.(注:羟基不能与碳碳双键中的碳原子直接相连)
考点:有机物的推断
专题:有机物的化学性质及推断
分析:由题意可知2-丁烯经一系列反应之后生成F应为醇,则F是3,4-二甲基-3-己醇,F发生消去反应生成G,G和溴发生加成反应生成H,H和氢氧化钠溶液发生取代反应生成I,I和酸发生酯化反应生成J,J物质具有对称性,所以G为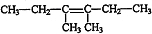 ,H为
,H为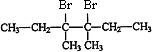 ,I为
,I为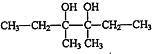 ,F为
,F为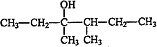 ,E为
,E为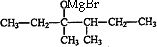 ,D为
,D为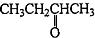 ,C为
,C为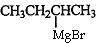 ,B为
,B为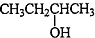 ,A为
,A为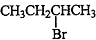 ,I和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,则J的结构简式为:
,I和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,则J的结构简式为: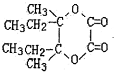 ,结合有机物的结构和性质以及题目要求可解答该题.
,结合有机物的结构和性质以及题目要求可解答该题.
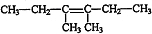 ,H为
,H为 ,I为
,I为 ,F为
,F为 ,E为
,E为 ,D为
,D为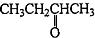 ,C为
,C为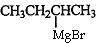 ,B为
,B为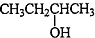 ,A为
,A为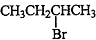 ,I和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,则J的结构简式为:
,I和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,则J的结构简式为: ,结合有机物的结构和性质以及题目要求可解答该题.
,结合有机物的结构和性质以及题目要求可解答该题.解答:
解:由题意可知2-丁烯经一系列反应之后生成F应为醇,则F是3,4-二甲基-3-己醇,F发生消去反应生成G,G和溴发生加成反应生成H,H和氢氧化钠溶液发生取代反应生成I,I和酸发生酯化反应生成J,J物质具有对称性,所以G为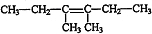 ,H为
,H为 ,I为
,I为 ,F为
,F为 ,E为
,E为 ,D为
,D为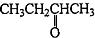 ,C为
,C为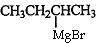 ,B为
,B为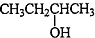 ,A为
,A为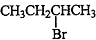 ,I和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,则J的结构简式为:
,I和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,则J的结构简式为: ,
,
(1)B为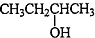 ,用系统命名法命名为:2-丁醇,故答案为:2-丁醇;
,用系统命名法命名为:2-丁醇,故答案为:2-丁醇;
(2) 和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,故答案为:HOOC-COOH;
和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,故答案为:HOOC-COOH;
(3)反应①③⑥为加成反应,反应②④⑦⑧属于取代反应,反应⑤属于消去反应,
故答案为:D;A;
(4)B→D的反应方程式为:2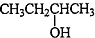 +O2
+O2
2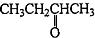 +2H2O;
+2H2O;
I→J的反应方程式为: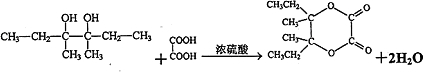 ,
,
故答案为:2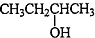 +O2
+O2
2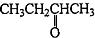 +2H2O;
+2H2O; ;
;
(5)D为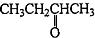 ,D的同分异构体符合以下条件:①能与Na反应反出H2,说明含有-OH;③有二种官能团,还含有碳碳双键;②核磁共振氢谱有四组峰,分子中有4种化学环境不同的H原子,且羟基不能与碳碳双键中的碳原子直接相连,符合条件的同分异构体为:CH2=C(CH3)CH2OH,
,D的同分异构体符合以下条件:①能与Na反应反出H2,说明含有-OH;③有二种官能团,还含有碳碳双键;②核磁共振氢谱有四组峰,分子中有4种化学环境不同的H原子,且羟基不能与碳碳双键中的碳原子直接相连,符合条件的同分异构体为:CH2=C(CH3)CH2OH,
故答案为:CH2=C(CH3)CH2OH.
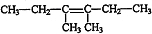 ,H为
,H为 ,I为
,I为 ,F为
,F为 ,E为
,E为 ,D为
,D为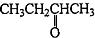 ,C为
,C为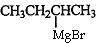 ,B为
,B为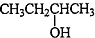 ,A为
,A为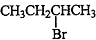 ,I和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,则J的结构简式为:
,I和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,则J的结构简式为: ,
,(1)B为
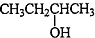 ,用系统命名法命名为:2-丁醇,故答案为:2-丁醇;
,用系统命名法命名为:2-丁醇,故答案为:2-丁醇;(2)
 和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,故答案为:HOOC-COOH;
和二元酸发生酯化反应生成J(C10H16O4)具有六元环,可知该二元酸为HOOC-COOH,故答案为:HOOC-COOH;(3)反应①③⑥为加成反应,反应②④⑦⑧属于取代反应,反应⑤属于消去反应,
故答案为:D;A;
(4)B→D的反应方程式为:2
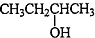 +O2
+O2| Cu |
| △ |
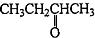 +2H2O;
+2H2O;I→J的反应方程式为:
 ,
,故答案为:2
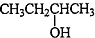 +O2
+O2| Cu |
| △ |
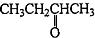 +2H2O;
+2H2O; ;
;(5)D为
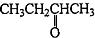 ,D的同分异构体符合以下条件:①能与Na反应反出H2,说明含有-OH;③有二种官能团,还含有碳碳双键;②核磁共振氢谱有四组峰,分子中有4种化学环境不同的H原子,且羟基不能与碳碳双键中的碳原子直接相连,符合条件的同分异构体为:CH2=C(CH3)CH2OH,
,D的同分异构体符合以下条件:①能与Na反应反出H2,说明含有-OH;③有二种官能团,还含有碳碳双键;②核磁共振氢谱有四组峰,分子中有4种化学环境不同的H原子,且羟基不能与碳碳双键中的碳原子直接相连,符合条件的同分异构体为:CH2=C(CH3)CH2OH,故答案为:CH2=C(CH3)CH2OH.
点评:本题考查有机物的推断,注意结合题目信息,以F为突破口,用逆推的方法进行推断,答题时注意把握反应条件推断官能团的变化,题目难度较大.

练习册系列答案
相关题目
下列关于有机物的说法正确的是( )
| A、苯乙烯分子中所有原子可能在同一个平面上 |
| B、分子式为C7H8O且分子中有苯环有机物共有4种 |
| C、乙醇和甘油互为同系物 |
| D、除去乙醇中混有的甲烷,可将混合气体通过酸性高锰酸钾溶液 |
下列有关物质的性质与应用不相对应的是( )
| A、CaH2能与水反应生成H2,可用作野外制氢气 |
| B、NH3具有还原性,可与灼热的CuO反应制备少量氮气 |
| C、SO2具有还原性,可使酸性高锰酸钾溶液褪色 |
| D、Si能导电,可用于制作光导纤维 |
 ,合成路线如下
,合成路线如下