题目内容
【题目】下表为元素周期表的一部分。请回答下列问题:
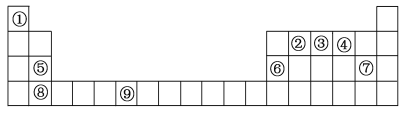
(1)上述元素中,属于s区的是__________ (填元素符号)。
(2)写出元素⑨的基态原子的价电子排布图________。
(3)元素的第一电离能:③________④(选填“大于”或“小于”)。
(4)元素③气态氢化物的VSEPR模型为________;该分子为________分子(选填“极性”或“非极性”)。
【答案】H、Mg、Ca ![]() 大于 四面体 极性
大于 四面体 极性
【解析】
根据元素在周期表中的位置可知,①~⑨这九种元素分别是H、C、N、O、Mg、Al、Cl、Ca、Cr元素。结合元素周期律和原子结构分析解答。
(1)上述元素中,属于s区的元素位于第I、IIA族,所以位于s区的元素是H、Mg、Ca,故答案为:H、Mg、Ca;
(2)元素⑨是Cr元素,为24号元素,其基态原子价电子为3d、4s能级上电子,3d、4s能级上分别含有5个和1个电子,所以其价电子排布图为![]() ,故答案为:
,故答案为:![]() ;
;
(3)同一周期元素,元素的第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族第一电离能大于其相邻元素,所以第一电离能N>O,故答案为:大于;
(4)元素③的气态氢化物是氨气,氨气分子中N原子价层电子对个数是4,含有一个孤电子对,根据价层电子对互斥理论,其VSEPR模型为四面体形;正负电荷重心重合的分子是非极性分子,不重合的分子是极性分子,氨气的空间构型为三角锥形,分子中正负电荷重心不重合,为极性分子,故答案为:四面体;极性;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目