题目内容
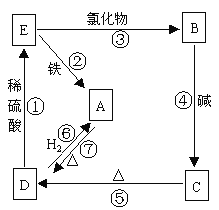
【题目】物质A可发生如图所表示的反应:
写出相应物质的化学式和类别(填在表格内),并依次写出各步反应的化学方程式。
A | B | C | D | E | |
化学式 | Cu | CuCl2 | ____ | ____ | ____ |
类 别 | _____ | _____ | 碱 | 氧化物 | 盐 |
(1)______________________________。
(2)______________________________。
(3)______________________________。
(4)______________________________。
(5)______________________________。
(6)______________________________ 。
(7)______________________________
【答案】单质 盐 Cu(OH)2 CuO CuSO4 CuO+H2SO4=CuSO4+H2O CuSO4+Fe=FeSO4+Cu CuSO4+BaCl2=BaSO4↓+CuCl2 CuCl2+2NaOH=Cu(OH)2↓+2NaCl Cu(OH)2![]() CuO+H2O CuO+H2
CuO+H2O CuO+H2![]() Cu+H2O 2Cu+O2
Cu+H2O 2Cu+O2![]() 2CuO
2CuO
【解析】
根据物质的定义判断物质所属类别,根据含有元素的种类及类别写出相应物质的化学式,然后写出符合题意的相应的化学反应方程式。
仅含有Cu元素一种元素的物质是金属Cu单质,则A是单质,B是CuCl2,C是碱,含有Cu元素,则C为Cu(OH)2,D是含有Cu元素的氧化物,D与硫酸反应产生盐,则D为CuO,E是CuO与硫酸反应产生的盐,则E是CuSO4,Cu与Cl2在点燃情况下反应产生CuCl2。
(1)反应①是CuO与稀硫酸反应产生CuSO4、H2O,反应方程式为CuO+H2SO4=CuSO4+H2O;
(2)反应②是CuSO4与Fe反应产生FeSO4、Cu,反应方程式为CuSO4+Fe=FeSO4+Cu;
(3)反应③是CuSO4与金属氯化物反应产生CuCl2,根据复分解反应的规律,金属氯化物为BaCl2,二者反应产生BaSO4沉淀和CuCl2,反应方程式为CuSO4+BaCl2=BaSO4↓+CuCl2;
(4)反应④是CuCl2与碱反应产生Cu(OH)2沉淀,碱可以是NaOH,则该反应方程式为CuCl2+2NaOH=Cu(OH)2↓+2NaCl;
(5)反应⑤是Cu(OH)2加热分解产生CuO、H2O,反应方程式为Cu(OH)2![]() CuO+H2O;
CuO+H2O;
(6)反应⑥是CuO与H2在加热条件下反应氧化还原反应产生Cu、H2O,反应方程式为CuO+H2![]() Cu+H2O;
Cu+H2O;
(7)反应⑦是Cu与O2加热产生CuO,反应方程式为:2Cu+O2![]() 2CuO。
2CuO。

【题目】某实验小组用粗锌(杂质难溶于水且不与酸反应)与100g稀硫酸反应时,实验数据如下表所示:
实验序号 | 粗锌质量/g | 稀硫酸质量/g | 生成气体质量/g | 反应后剩余固体质量/g |
实验1 | 8 | 100 | 0.2 | 1.5 |
实验2 | 16 | 100 | 0.4 | 3 |
实验3 | 30 | 100 | 0.6 | 10.5 |
(1)实验中稀硫酸反应完的是______(填实验序号);
(2)计算稀硫酸的溶质质量分数______。
【题目】实验室有一瓶未知浓度的Na2S2O3,通过下列实验测定其浓度
①取10.0 mL Na2S2O3于锥形瓶中,滴入指示剂2—3滴。
②取一滴定管,依次查漏,洗涤,用0.01 mol·L-1的I2溶液润洗,然后注入该标准溶液,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3 =2NaI+Na2S4O6。
试回答下列问题:
(1)步骤①加入的指示剂是__________。
(2)步聚③达到滴定终点的判断__________________________________。
(3)己知消耗标准液实验数据如下表:
实验次数 | 始读数(ml) | 末读数(ml) |
1 | 0.10 | 19.20 |
2 | 1.85 | 20.75 |
3 | 0.00 | 24.06 |
则废水中的Na2S2O3物质的量浓度为_______________。
(4) 下列操作会导致测定结果偏高的是_________。
A.滴定管在装液前未用标准溶液润洗
B.滴定过程中,锥形瓶振荡得太剧烈,锥形瓶内有液滴溅出
C.装标准溶液的滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数