题目内容
【题目】根据我国目前汽车业发展速度,预计![]() 年汽车保有量超过
年汽车保有量超过![]() 亿辆,中国已成为全球最大的汽车市场。因此,如何有效处理汽车排放的尾气,是需要进行研究的一项重要课题。
亿辆,中国已成为全球最大的汽车市场。因此,如何有效处理汽车排放的尾气,是需要进行研究的一项重要课题。
(1)目前,汽车厂商常利用催化技术将尾气中的![]() 和
和![]() 转化成
转化成![]() 和
和![]() ,化学方程式为:_______________;
,化学方程式为:_______________;
为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究:
(资料查阅)①不同的催化剂对同一反应的催化效率不同;
②使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率有影响.
(实验设计)课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。
(2)完成以下实验设计表(表中不要留空格)。
实验编号 | 实验目的 | T / ℃ |
|
| 同种催化剂的比表面积
|
| 为以下实验作参照 |
|
|
|
|
| ①___________ | 280 |
|
|
|
| 探究温度对尾气转化速率的影响 |
| ②_________ |
|
|
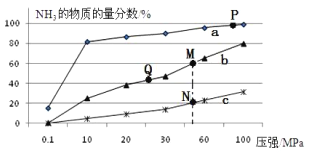
(图象分析与结论)利用气体传感器测定了三组实验中![]() 浓度随时间变化的曲线图,如图:
浓度随时间变化的曲线图,如图:

(3)计算第![]() 组实验中,达平衡时
组实验中,达平衡时![]() 的浓度为________;
的浓度为________;
(4)由曲线![]() 、
、![]() 可知,增大催化剂比表面积,汽车尾气转化速率____________________(填“增大”、“减小”、“无影响”)。
可知,增大催化剂比表面积,汽车尾气转化速率____________________(填“增大”、“减小”、“无影响”)。
(5)下列措施中,能减少或控制汽车尾气污染有效且可行的是________.
A.制定严格的汽车尾气排放标准,并严格执行
B.开发清洁能源汽车,如氢能汽车、太阳能汽车等
C.将污染源移到人口密集度低的郊区
【答案】2NO + 2CO![]() 2CO2 + N2 探究催化剂比表面积对尾气转化速率的影响 6.50×10—3 3.50×10—3 mol/L 增大 AB
2CO2 + N2 探究催化剂比表面积对尾气转化速率的影响 6.50×10—3 3.50×10—3 mol/L 增大 AB
【解析】
(1)利用催化技术将尾气中的NO和CO转化成氮气和二氧化碳,反应的化学方程式为2NO+2CO![]() 2CO2+N2;
2CO2+N2;
(2)影响反应速率的因素有浓度、压强、温度和催化剂的比表面积,而要想探究一种影响因素,必须保持其他影响因素是一致;Ⅰ、Ⅱ比较不同的是催化剂的比表面积,则实验目的是探究催化剂比表面积对尾气转化速率的影响;Ⅲ是探究温度对尾气转化速率的影响,温度是变量,其余保持不变,则NO的初始浓度为6.50×10—3mol/L;
(3)通过图象可知,第Ⅰ组实验中达到平衡时CO的平衡浓度为1.00×10—3mol/L,可得出CO的浓度该变量△C(CO)=4.00×10—3mol/L-1.00×10—3 mol/L=3.00×10—3 mol/L,在一个反应中,各物质的浓度的该变量之比等于计量数之比,故NO的浓度的该变量△c(NO)=3.00×10—3mol/L,故NO的平衡浓度c(NO)=6.50×10—3 mol/L-3.00×10—3mol/L=3.50×10—3mol/L;
(4)由图象可知,增大催化剂比表面积后,缩短了到达平衡的时间,故增大了反应速率。
(5)A.制定严格的汽车尾气排放标准,并严格执行,能减少或控制汽车尾气污染,A正确;
B.开发清洁能源汽车,如氢能汽车、太阳能汽车等,能减少或控制汽车尾气污染,B正确;
C.将污染源移到人口密集度低的郊区,不能减少或控制汽车尾气污染,C错误;
答案选AB。

 阅读快车系列答案
阅读快车系列答案