题目内容
【题目】在0.1mol/LCH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+对于该平衡,下列叙述正确的是( )
CH3COO-+H+对于该平衡,下列叙述正确的是( )
A. 加入水时,平衡向逆反应方向移动
B. 加入少量NaOH固体,平衡向正反应方向移动
C. 加入少量0.1mol·L-1 HCl溶液,溶液中c(H+)减小
D. 加入少量CH3COONa固体,平衡向正反应方向移动
【答案】B
【解析】0.1mol/L CH3COOH溶液中存在水解平衡为CH3COOH+H2O![]() CH3COO—+H3O+。A项加入水时,平衡正反应方向移动,错误;B项加入少量的NaOH固体,则会消耗溶液中的H+,平衡向正反应方向移动,正确;C项,、加入少量0.1 mol/L HCl溶液,平衡虽然会向逆反应方向移动,但溶液中C(H+)增大,错误;加入少量CH3COONa 固体,溶液中的CH3COO—的浓度增大,平衡向逆反应方向移动,错误。
CH3COO—+H3O+。A项加入水时,平衡正反应方向移动,错误;B项加入少量的NaOH固体,则会消耗溶液中的H+,平衡向正反应方向移动,正确;C项,、加入少量0.1 mol/L HCl溶液,平衡虽然会向逆反应方向移动,但溶液中C(H+)增大,错误;加入少量CH3COONa 固体,溶液中的CH3COO—的浓度增大,平衡向逆反应方向移动,错误。

 阅读快车系列答案
阅读快车系列答案【题目】有着“植物大熊猫”和世界上最长寿树种美称、在地球上已有250万年历史的红豆杉,入选2010年世博会中国馆珍稀植物展出品种。在活的红豆杉植株体内含量最多的化学元素是( )
A.CB.HC.ND.O
【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | 85.5 | 115.2 | >600(分解) | 75.5 | 16.8 | 10.3 |
沸点/℃ | 60.3 | 444.6 | 10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为__________,基态S原子电子占据最高能级的电子云轮廓图为_________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_________。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________。
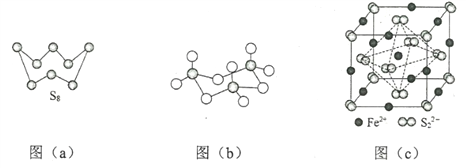
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为_____形,其中共价键的类型有______种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm3;晶胞中Fe2+位于![]() 所形成的正八面体的体心,该正八面体的边长为______nm。
所形成的正八面体的体心,该正八面体的边长为______nm。



