题目内容
反应N2O4(g)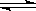 2NO2(g)⊿H = +57KJ/mol,在温度为
2NO2(g)⊿H = +57KJ/mol,在温度为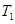 、
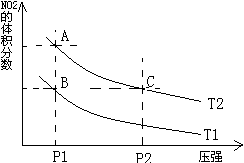
、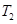 时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 ( )
时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 ( )
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.由状态B到状态A,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C
 2NO2(g)⊿H = +57KJ/mol,在温度为
2NO2(g)⊿H = +57KJ/mol,在温度为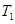 、
、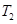 时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 ( )
时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 ( )
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.由状态B到状态A,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C
C
A、C两点:在相同温度下,P2>P1,则应υ(C) >υ(A),故A错误;
由于C点压强大,那么容器体积是减小的,所以气体被压缩,则看起来C点颜色深了,尽管C中NO2的体积分数比A小,但是平衡移动是微弱的,比不过体积改变对颜色的影响,故B错误;
C项,加热,平衡右移,正确;
平均相对分子质量=气体总质量/气体总物质的量,气体总质量不变,而由A点到C点,压强增大,平衡左移,所以气体总物质的量减小,则气体的平均相对分子质量增大,即:C>A,故D错误;
由于C点压强大,那么容器体积是减小的,所以气体被压缩,则看起来C点颜色深了,尽管C中NO2的体积分数比A小,但是平衡移动是微弱的,比不过体积改变对颜色的影响,故B错误;
C项,加热,平衡右移,正确;
平均相对分子质量=气体总质量/气体总物质的量,气体总质量不变,而由A点到C点,压强增大,平衡左移,所以气体总物质的量减小,则气体的平均相对分子质量增大,即:C>A,故D错误;

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
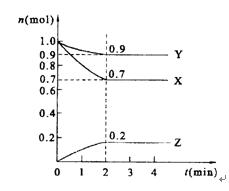
 C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1,c(B)="0.200" mol·L-1, c(C)="0" mol·L-1。反应物A的浓度随时间的变化如图所示。下列说法正确的是
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1,c(B)="0.200" mol·L-1, c(C)="0" mol·L-1。反应物A的浓度随时间的变化如图所示。下列说法正确的是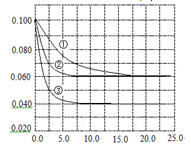
 2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是
2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是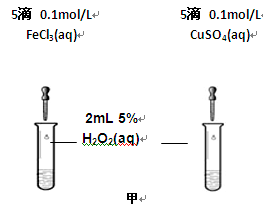
 1/2N2(g)+CO2(g)△H="-373.2" kJ/mol。达到平衡后,为了提高该反应的速率和NO的转换率,采取的措施正确的是( )
1/2N2(g)+CO2(g)△H="-373.2" kJ/mol。达到平衡后,为了提高该反应的速率和NO的转换率,采取的措施正确的是( )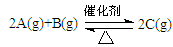 过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:
过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表: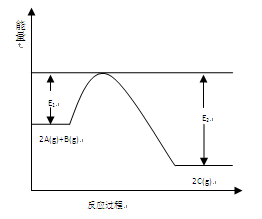
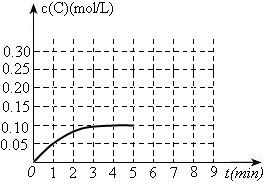
 2NH3,已达平衡状态的是( )
2NH3,已达平衡状态的是( )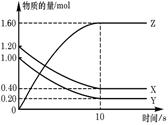
 2Z(g),平衡常数K=4
2Z(g),平衡常数K=4