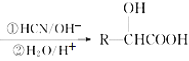题目内容
【题目】常温下,向1L0.01mol·L-1一元酸HR溶液中逐渐通入氨气[常温下NH3·H2O电离平衡常数K=1.76×10-5],保持温度和溶液体积不变,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述不正确的是
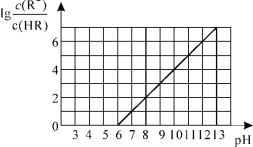
A.0.01mol·L-1HR溶液的pH约为4
B.随着氨气的通入,![]() 逐渐减小
逐渐减小
C.当溶液为碱性时,c(R-)>c(HR)
D.当通入0.01 mol NH3时,溶液中存在:c(R-)>c(NH4+)>c(H+)>c(OH-)
【答案】D
【解析】
A. pH=6时c(H+)=10-6,由图可得此时![]() =0,则Ka=
=0,则Ka= =10-6,设HR 0.01mol·L-1电离了X mol·L-1,Ka=
=10-6,设HR 0.01mol·L-1电离了X mol·L-1,Ka=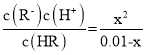 =10-6 ,解得X=10-6,pH=4,A项正确;
=10-6 ,解得X=10-6,pH=4,A项正确;
B. 由已知HR溶液中存在着HR分子,所以HR为弱酸,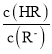 =
=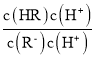 = c(H+)/Ka温度不变时Ka的值不变,c(H+)浓度在减小,故
= c(H+)/Ka温度不变时Ka的值不变,c(H+)浓度在减小,故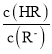 在减小,B项正确;
在减小,B项正确;
C.当溶液为碱性时,R-的水解会被抑制,c(R-)>c(HR),C项正确;
D. Ka=10-6,当通入0.01 mol NH3时,恰好反应生成NH4R,又因为常温下NH3·H2O电离平衡常数K=1.76×10-5,所以NH4R溶液中R-水解程度大于NH4+水解程度,NH4R溶液呈碱性,则c(NH4+)>c(R-)>c(OH-)>c(H+),D项错误;
答案选D。

练习册系列答案
 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目