题目内容
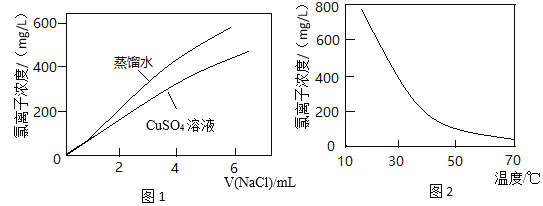
【题目】图1表示:以相同的滴速分别向同体积的蒸馏水和0.1 mol/L CuSO4溶液中滴入NaCl溶液,氯离子浓度随氯化钠加入量的变化关系。图2表示:CuCl2溶液中氯离子浓度随温度变化关系。结合信息,下列推断不合理的是
已知:CuSO4溶液中存在平衡X:Cu2++4H2O![]() [Cu(H2O)4]2+(蓝色)
[Cu(H2O)4]2+(蓝色)
CuCl2溶液呈绿色,溶液中存在平衡Y:4Cl-+[Cu(H2O)4]2+![]() [CuCl4]2-+4H2O
[CuCl4]2-+4H2O
A.平衡Y是图1中两条曲线没有重合的主要原因
B.由图2可知平衡Y为吸热反应
C.平衡X是无水硫酸铜粉末和硫酸铜溶液颜色不同的原因
D.CuCl2溶液加水稀释,溶液最终变为浅绿色
【答案】D
【解析】
A.以相同的滴加速度滴加相同浓度的NaCl溶液,CuSO4溶液中Cl-浓度增加的慢,是由于发生反应Y,消耗了Cl-,A正确;
B.由图2可知:升高温度,CuCl2溶液中氯离子浓度降低,说明升高温度,化学平衡4Cl-+[Cu(H2O)4]2+![]() [CuCl4]2-+4H2O正向移动;根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动,该反应的正反应为吸热反应,B正确;
[CuCl4]2-+4H2O正向移动;根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动,该反应的正反应为吸热反应,B正确;
C.无水硫酸铜粉末是白色固体,当固体溶于水时,与水发生反应产生[Cu(H2O)4]2+,使溶液显蓝色,因此平衡X的存在导致无水硫酸铜粉末和硫酸铜溶液显示不同的颜色,C正确;
D.CuCl2溶液呈绿色,加水稀释,4Cl-+[Cu(H2O)4]2+![]() [CuCl4]2-+4H2O的平衡逆向移动,[Cu(H2O)4]2+的浓度增大,溶液会逐渐变为蓝色,D错误;
[CuCl4]2-+4H2O的平衡逆向移动,[Cu(H2O)4]2+的浓度增大,溶液会逐渐变为蓝色,D错误;
故答案选D。

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目