题目内容
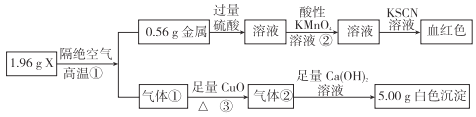
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:

(1)固体I中主要成分为__________,捕获剂所捕获的气体主要是_________。
(2)处理含NH4+废水时,发生反应的离子方程式为___________。
(3)若X为适量空气,严格控制空气用量的原因是____________。
(4)工业废气中的SO2、NO还可采用NaClO2溶液作为吸收剂进行净化,在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表:
离子 | SO42- | SO32- | NO3- | NO2- | Cl- |
c(mol·L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式_________________。
增加压强,NO的转化率__________(填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐__________(填“增大”、“不变”或“减小”)。
③如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是_______________。
【答案】 CaCO3 CaSO3 Ca(OH)2 CO NH4++NO2-=N2+2H2O 过量空气会将NO氧化成NO3-,无法与NH4+发生反应 4NO+3ClO2-+4OH-=4NO3-+3Cl-+2H2O 提高 减小 Ca2+与SO42-结合生成CaSO4沉淀,使平衡向产物方向移动,SO2转化率提高
【解析】工业废气中CO2、SO2可被石灰水吸收,生成CaCO3、CaSO3,气体a是不能被过量石灰水吸收的N2、NO、CO,气体a通入空气,用氢氧化钠溶液处理后到的NaNO2,通入空气但不能过量,否则得到硝酸钠,NaNO2与含有NH4+的溶液反应生成无污染气体,应生成氮气,则气体b含有CO、N2,经捕获剂得到氮气,防止污染空气,因此捕获剂所捕获的气体主要是CO。
(1)工业废气中CO2、SO2可被石灰水吸收,生成CaCO3、CaSO3,因氢氧化钙过量,则废渣的成分为主要含有CaCO3、CaSO3、Ca(OH)2,气体b含有CO、N2,捕获剂所捕获的气体主要是CO,故答案为:CaCO3、CaSO3、Ca(OH)2;CO;
(2)NaNO2与含有NH4+的溶液反应生成无污染气体,应生成氮气,发生氧化还原反应,离子方程式为:NH4++NO2-=N2↑+2H2O,故答案为:NH4++NO2-=N2↑+2H2O;
(3)由分析可知,气体1是不能被过量石灰水吸收的N2、NO、CO,气体a通入空气,用氢氧化钠溶液处理后到的NaNO2,通入的空气不能过量,过量空气会将NO氧化成NO3-,无法与NH4+发生反应,故答案为:过量空气会将NO氧化成NO3-,无法与NH4+发生反应;
(4)①亚氯酸钠具有氧化性,且NaClO2溶液呈碱性,则NaClO2溶液脱硝过程中主要反应的离子方程式为3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O;正反应是体积减小的反应,则增加压强,NO的转化率提高,故答案为:3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O;提高;
②根据反应的方程式3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O可知随着吸收反应的进行氢氧根离子被消耗,吸收剂溶液的pH逐渐降低,故答案为:减小;
③如果采用NaClO、Ca(ClO)2替代NaClO2,生成硫酸钙沉淀,降低硫酸根离子浓度,促使平衡向正反应方向进行,所以Ca(ClO)2效果好,故答案为:形成CaSO4沉淀,降低硫酸根离子浓度,反应平衡向产物方向移动,SO2转化率提高。