题目内容
【题目】亚硝酸钠是一种工业盐,在生产、生活中应用广泛。现用下图所示装置(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
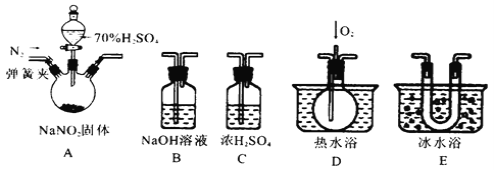
已知:① NO+NO2+2OH-=2NO2-+H2O
② 气体液化的温度:NO2(21℃)、NO(–152℃)
(1)反应前应打开弹簧夹,先通入一段时间氮气,目的是________________________。
(2)为了检验装置A中生成的气体产物,仪器的连接顺序为(从左向右连接):A→_____________;组装好仪器后,接下来进行的操作是________________。
(3)关闭弹簧夹,打开分液漏斗活塞,滴入70%的硫酸后,A中产生红棕色气体。
① 确认A中产生气体含有NO,依据的现象是_____________________________。
② 装置E的作用是_______________________________________________________。
(4)如果没有装置C,对实验结论造成的影响是______________________________。
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是_______________。
【答案】 排出装置中的空气,防止干扰NO的检验 CEDB 检查装置的气密性 D中有红棕色气体生成 冷凝,使NO2完全液化 水会与NO2生成NO,影响NO的检验 2NaNO2 + H2SO4 = Na2SO4 + NO2↑ + NO↑ + H2O
【解析】(1)反应前应打开弹簧夹,先通入一段时间氮气,排出装置中的空气,防止干扰NO的检验,否则也会影响NO和NO2的检验;(2)为了检验装置A中生成的气体产物,仪器的连接顺序为(从左向右连接):A是发生装置,C是干燥除去水,NO和NO2的分离,因为NO2更易液化,先分离NO2,所以接E冷却二氧化氮,NO2分离后再检验NO,再接D通氧气,观察到气体从无色变成红棕色,说明是NO,B是尾气处理;吸收反应后剩余的NO和NO2的混合气体,防止污染空气。装置的连接为A→C→E→D→B;有气体参与或生成的实验必须检查装置的气密性,故组装好仪器后,接下来进行的操作是检查装置的气密性;(3)关闭弹簧夹,打开分液漏斗活塞,滴入70%的硫酸后, A中产生红棕色气体。说明生成了NO2气体。①确认A中产生气体含有NO,是在D装置中通O2来检验的。观察D中有红棕色气体生成;②装置E的作用是冷凝,是使NO2完全液化;(4)如果没有装置C则没有对气体干燥,水会与NO2反应产生NO,影响NO的检验;(5)通过上述实验探究过程,可得出装置A中NaNO2 和70%的H2SO4 反应生成Na2SO4 、 NO2、 NO等物质,反应的化学方程式是:2NaNO2 + H2SO4 = Na2SO4 + NO2↑ + NO↑ + H2O。

 名校课堂系列答案
名校课堂系列答案