题目内容
【题目】【化学﹣物质结构与性质】 钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
(1)钛有2248和2250Ti两种原子,它们互称为 . Ti元素在元素周期表中的位置是第周期,第族;基态原子的电子排布式为按电子排布Ti元素的元素周期表分区中属于区元素.
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如图所示,它的化学式是 . 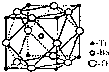
(3)现有含Ti3+的配合物,化学式为[TiCl(H2O)5]Cl2H2O.配离子[TiCl(H2O)5]2+中含有的化学键类型是 , 该配合物的配体是 .
【答案】
(1)同位素;四;IVB;Is22s22p63S23p63d24s2(或[Ar]3d24s2);d
(2)BaTiO3
(3)极性共价键(或共价键)、配位键;H2O、Cl﹣
【解析】解:(1)2248Ti和2250Ti的质子数相同而中子数不同,是钛元素的不同原子,互为同位素,钛元素在周期表中的原子序数为21,位于第四周期第、IVB族,基态原子的电子排布式为Is22s22p63S23p63d2 4s2(或[Ar]3d24s2),在d区,所以答案是:同位素;四;IVB;Is22s22p63S23p63d24s2(或[Ar]3d24s2);d;(2)晶胞中分摊的各种原子的数目之比Ba:Ti:O=1:(8× ![]() ):(12×
):(12× ![]() )=1:1:3,故分子式为:BaTiO3 , 所以答案是:BaTiO3;(3)配离子[TiCl(H2O)5]2+中含有非金属原子之间的极性共价键以及配位键,钛元素的配位体是H2O、Cl﹣ , 所以答案是:极性共价键(或共价键);H2O、Cl﹣ .
)=1:1:3,故分子式为:BaTiO3 , 所以答案是:BaTiO3;(3)配离子[TiCl(H2O)5]2+中含有非金属原子之间的极性共价键以及配位键,钛元素的配位体是H2O、Cl﹣ , 所以答案是:极性共价键(或共价键);H2O、Cl﹣ .

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。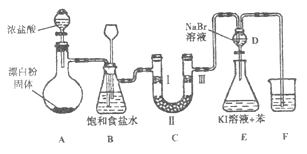
(1)装置A是氯气的发生装置,请写出该反应相应的化学方程式:。
(2)装置B中饱和食盐水的作用是;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、Ⅱ、Ⅲ处依次放入物质的组合应是(填字母编号)。
编号 | I | Ⅱ | Ⅲ |
a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是 , 该现象(填“能”或“不能”) 说明溴单质的氧化性强于碘,原因是。
(5)装置F的烧杯中的溶液不能选用下列中的(填字母编号)。a.饱和NaOH溶液 b.饱和Ca(OH)2溶液 c.饱和Na2CO3溶液