题目内容
下列物质的转化在指定条件下能实现的是
①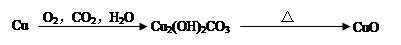
②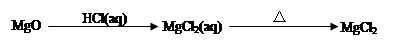
③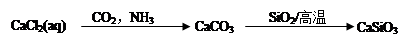
④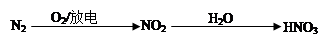
⑤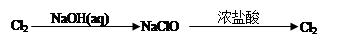
①
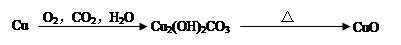
②
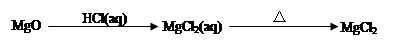
③
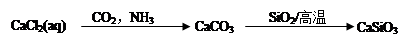
④
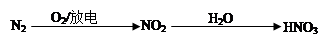
⑤
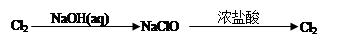
| A.①④⑤ | B.①③⑤ | C.②③⑤ | D.①②④ |
B
试题分析:②MgCl2溶液到MgCl2固体需要在酸性条件下脱水,错误;④中氮气在放电条件下与氧气生成NO不能生成NO2,错误;

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
题目内容
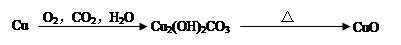
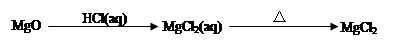
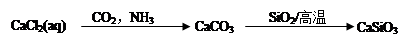
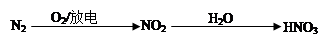
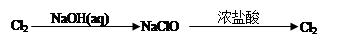
| A.①④⑤ | B.①③⑤ | C.②③⑤ | D.①②④ |

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案