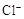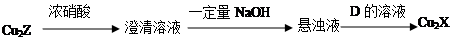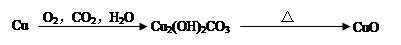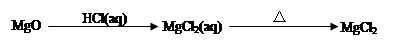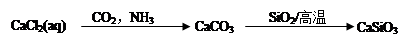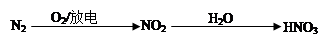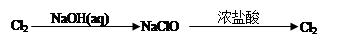题目内容
下列叙述正确的是
| A.NaHCO3固体中既含有离子键,又含有共价键,溶于水后的电离方程式为 NaHCO3=Na++H++CO32- |
B.符合a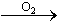 b b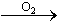 c转化关系的单质a可以是N2、Al、Si、S c转化关系的单质a可以是N2、Al、Si、S |
| C.室温下,pH=3的溶液中,Na+、Fe2+、NO3-、AlO2-四种离子不能大量共存 |
| D.用焰色反应或澄清石灰水均可鉴别Na2CO3与KHCO3溶液 |
C
试题分析:A、碳酸氢钠是弱酸的酸式盐,其电离方程式是NaHCO3=Na++HCO3-,A不正确;B、N2+O2=2NO、2NO+O2=2NO2;4Al+3O2=2Al2O3,氧化铝与氧气不反应;Si+O2=SiO2,二氧化硅与氧气不反应;S+O2=SO2、2SO2+O2=2SO3,所以选项B不正确;C、室温下,pH=3的溶液显酸性,则AlO2-不大量共存。在酸性条件下,NO3-能氧化Fe2+不能大量共存,C正确;D、Na2CO3与KHCO3溶液均能和澄清石灰水反应生成白色沉淀碳酸钙,不能鉴别,D不正确,答案选C。

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
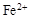 >
>