题目内容
(6分)将6 mol H2和3 mol CO充入容积为1 L的密闭容器中,进行如下反应:2 H2(气) + CO(气) 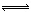 CH3OH(气),6秒时体系达到平衡,此时容器内压强为开始时的0.6倍,求:(1)H2的反应速率;(2)CO的转化率;(3)求相同条件下CH3OH(气)
CH3OH(气),6秒时体系达到平衡,此时容器内压强为开始时的0.6倍,求:(1)H2的反应速率;(2)CO的转化率;(3)求相同条件下CH3OH(气) 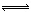 2 H2(气) + CO(气)的平衡常数K
2 H2(气) + CO(气)的平衡常数K
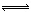 CH3OH(气),6秒时体系达到平衡,此时容器内压强为开始时的0.6倍,求:(1)H2的反应速率;(2)CO的转化率;(3)求相同条件下CH3OH(气)
CH3OH(气),6秒时体系达到平衡,此时容器内压强为开始时的0.6倍,求:(1)H2的反应速率;(2)CO的转化率;(3)求相同条件下CH3OH(气) 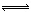 2 H2(气) + CO(气)的平衡常数K
2 H2(气) + CO(气)的平衡常数K 2 H2(气) + CO(气) 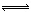 CH3OH(气)
CH3OH(气)
起始量(mol) 6 3 0
转化量(mol) 2x x x
平衡量(mol) 6-2x 3-x x
因为压强之比是物质的量之比
所以有(6+3)×0.6=(6-2x+3-x+x)
解得x=1.8mol
所以(1)氢气的反应速率是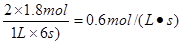
(2)CO的转化率是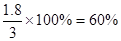
该反应的平衡常数为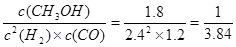
因为逆反应的平衡常数是正反应的平衡常数的倒数
所以(3)相同条件下CH3OH(气)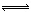 2 H2(气) + CO(气)的平衡常数K=3.84。
2 H2(气) + CO(气)的平衡常数K=3.84。
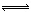 CH3OH(气)
CH3OH(气)起始量(mol) 6 3 0
转化量(mol) 2x x x
平衡量(mol) 6-2x 3-x x
因为压强之比是物质的量之比
所以有(6+3)×0.6=(6-2x+3-x+x)
解得x=1.8mol
所以(1)氢气的反应速率是
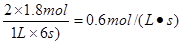
(2)CO的转化率是
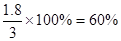
该反应的平衡常数为
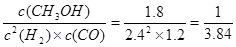
因为逆反应的平衡常数是正反应的平衡常数的倒数
所以(3)相同条件下CH3OH(气)
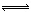 2 H2(气) + CO(气)的平衡常数K=3.84。
2 H2(气) + CO(气)的平衡常数K=3.84。考查可逆反应的有关计算。

练习册系列答案
相关题目
 2NH3(正反应为放热反应)达到平衡后,下列选项中三种方法都能使平衡向正反应方向移动的是( )
2NH3(正反应为放热反应)达到平衡后,下列选项中三种方法都能使平衡向正反应方向移动的是( ) nW(g) ΔH,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
nW(g) ΔH,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图: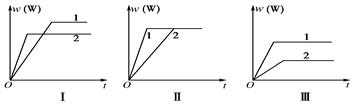
 3C(g)+D(g),达到平衡状态的是( )
3C(g)+D(g),达到平衡状态的是( ) pC(g),达到平衡时,测得c(C)为0.5 mol·L-1;在温度不变的条件下,将容器体积扩大一倍,当达到平衡时,测得c(C)为0.3 mol·L-1。则下列判断正确的是( )
pC(g),达到平衡时,测得c(C)为0.5 mol·L-1;在温度不变的条件下,将容器体积扩大一倍,当达到平衡时,测得c(C)为0.3 mol·L-1。则下列判断正确的是( ) 2SO3 ,这是一个正反应放热的可逆反应。下列有关说法中错误的是()
2SO3 ,这是一个正反应放热的可逆反应。下列有关说法中错误的是()