��Ŀ����
����Ŀ��һ�������£�CO2(g)+3H2(g)![]() H2O(g)+CH3OH(g) ��H=-53.7kJ/mol����2L ���ݺ����ܱ������г���1mol CO2��2.8molH2��Ӧ��ͼ�й���I�����������ֲ�ͬ���������½���ƽ��Ĺ�����CO2��ת����[��(CO2)]��ʱ��(t)�ı仯���ߡ�����˵������ȷ����
H2O(g)+CH3OH(g) ��H=-53.7kJ/mol����2L ���ݺ����ܱ������г���1mol CO2��2.8molH2��Ӧ��ͼ�й���I�����������ֲ�ͬ���������½���ƽ��Ĺ�����CO2��ת����[��(CO2)]��ʱ��(t)�ı仯���ߡ�����˵������ȷ����

A. m��:v(��)>v(��)
B. ��ܣ����̢�>����I
C. n��ʱ�÷�Ӧ��ƽ�ⳣ��K��50
D. ����I��t2ʱ�̸ı�ķ�Ӧ���������������¶�
���𰸡�C
��������A. m��CO2��ת���ʲ������Ӧ��������Ӧ������У����v(��)>v(��)��A��ȷ��B. ����I���ȴﵽƽ��״̬��˵����Ӧ���ʿ죬��˻�ܣ����̢�>����I��B��ȷ��C. n��ʱCO2��ת������0.8������ݷ���ʽ��֪
CO2(g)+3H2(g)![]() H2O(g)+CH3OH(g)
H2O(g)+CH3OH(g)
��ʼŨ�ȣ�mol/L�� 0.5 1.4 0 0
ת��Ũ�ȣ�mol/L�� 0.4 1.2 0.4 0.4
ƽ��Ũ����mol/L�� 0.1 0.2 0.4 0.4
���Ը÷�Ӧ��ƽ�ⳣ��K��![]() ��200��C������
��200��C������
D. ����I��t2ʱ��ת���ʽ��ͣ�˵����Ӧ���淴Ӧ������У���������Ӧ���ȣ���˸ı�ķ�Ӧ���������������¶���D��ȷ����ѡC��

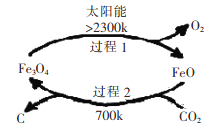
 ���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�����Ŀ��FeCl2��һ�ֳ��õĻ�ԭ�����й��������£�
C6H5Cl(�ȱ�) | C6H4Cl2 | FeCl3 | FeCl2 | |
�ܽ��� | ������ˮ�������ڱ� | ������C6H5Cl��C6H4Cl2����������ˮ�� | ||
�۵㣯�� | -45 | 53 | ���� | ���� |
�е㣯�� | 132 | 173 | ���� | ���� |
ʵ���ҿ����ö��ַ������Ʊ���ˮFeCl2���ش��������⣺
I������ͼlװ����H2��ԭ��ˮFeCl3��ȡ��װ��C��������_________��E��ʢ�ŵ��Լ���_________��D�з�Ӧ�Ļ�ѧ����ʽΪ_________��

II������ͼ2װ�ã���������ƿ�з���162.5g��ˮ�Ȼ�����225g�ȱ������Ʒ�Ӧ�¶���128��139������3h����Ӧ�ӽ�100%����ȴ�������ᴿ�õ��ֲ�Ʒ����Ӧ���£�2FeCl3+C6H5Cl��2FeCl2+C6H4Cl2+HC1
��1������ȡ��Ӧ�У�����ԭ������_________��
��2����Ӧ�¶Ƚӽ���C6H5Cl�ķе㣬��ʵ�������C6H5Cl�����������ʧ��ԭ����_________��
��3����ȴʵ��װ�ã�������ƿ�����ʾ������ˡ�ϴ�ӣ�������õ��ֲ�Ʒ��
��ϴ�����õ��Լ�������_________��
�ڻ�����Һ��C6H5Cl�ķ�����_________��
��4����ͨ���ձ��е�����仯�Ϳ��Լ���Ȼ�����ת��������Ҫ����Ȼ���ת���ʴﵽ��90%�����ձ����Լ������Ǽ��з�̪���������Ϻ�_________g NaOH����Һ��