��Ŀ����
����Ŀ������пƬ�ʹ�ͭƬ��ͼ��ʽ����100 mL��ͬŨ�ȵ�ϡ������һ��ʱ�䣬��ش��������⣺
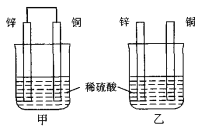
��1������˵����ȷ����________��
A���ס��Ҿ�Ϊ��ѧ��ת��Ϊ���ܵ�װ��
B������ͭƬ��û�����Ա仯
C������ͭƬ�������١�����пƬ��������
D�����ձ�����Һ��pH������
��2������ͬʱ���ڣ����ձ��в������ݵ��ٶȣ���____�ң�����������������������������
��3�������в���1.12L����״��������ʱ��ͨ�����ߵĵ�����ĿΪ__________��
��4�������в���1.12L����״��������ʱ����п��ͭƬȡ�����ٽ��ձ��е���Һϡ����1 L�������Һ��c(H��)��0.1 mol��L��1���跴Ӧǰ����Һ������䣩����ȷ��ԭϡ��������ʵ���Ũ��Ϊ______��
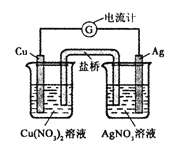
��5���������з�Ӧ��Fe��2Fe3+��3Fe2+��һ����ѧ��أ��������ɵ��ߺ�һ��С���ݣ��缫���Ϻ͵��Һ��ѡ��������ʵ��װ��ͼ��ע���������Һ���ƺ����������ϣ������������д���缫��Ӧʽ��___

_______��������������Ӧʽ��_____________��
________�Ǹ�����������Ӧʽ��____________
��6��1958�������ϵ�һ���������������ֲ������ɹ���ʹ����������10��֮�á�������Դ�����а�װ��������ɿ�����ߵ��һ̼��أ����ֵ��������ѹ�ȶ�������-56.7��71.1���¶ȷ�Χ�����������������ڻ�����ƶ��绰���ʼDZ������й㷺ʹ�á�������﮺�ʯī���缫�����Ȼ����(LiAlCl4)�ܽ�������������(SOCl2)��ɵ������Һ������ܷ�ӦΪ��8Li+3SOCl2=6LiCl+Li2SO3+2S���˵����__�������������ĵ缫��ӦΪ_______��
���𰸡�BD �� 6.02��1022 1mol/L  Cu 2Fe3++2e-=2Fe2+ Fe Fe-2e-=Fe2+ ʯī Li-e-=Li+
Cu 2Fe3++2e-=2Fe2+ Fe Fe-2e-=Fe2+ ʯī Li-e-=Li+
��������
��1����װ�÷���ԭ��ع���������������ԭ��أ��Ҳ����γɱպϻ�·�����Բ��ܹ���ԭ��أ������ձ��У�п��ʧ���ӷ���������Ӧ������ͭ�������ӵõ��ӷ�����ԭ��Ӧ������п�������ӵõ��ӷ�����ԭ��Ӧ��
��2����ԭ��ظ����Ľ������ٱ���ʴ��
��3������������ת�Ƶ���֮��Ĺ�ϵʽ���㣻
��4���ȼ��������ӵ����ʵ����ټ���Դϡ�����Ũ�ȣ�
��5����֪Fe+2Fe3+�T3Fe2+�����ݷ�Ӧ��֪FeӦΪ������ʧ���ӱ�������������ΪC��Cu�ȣ�������Fe3+�õ�������Fe2+���������Һ����Fe3+��
��6������ԭ���ԭ�����з�������
(1)A. ����ԭ��ع�����������������ԭ��أ��Ҳ��ܹ��ɱպϻ�·�����Բ��ܹ���ԭ��أ�A�����
B. �Ҳ��ܹ���ԭ��أ���������пƬ�ϵõ��ӷ�����ԭ��Ӧ����������ͭƬ��û�����Ա仯��B����ȷ��
C. ����ͭƬ�������������������ӵõ�����������������ͭƬ�������䣬����пƬ�������ӷ����û���Ӧ�������������٣�C�����
D. ���ձ���п�������ӷ����û���Ӧ������Һ��������Ũ�ȼ�С��������Һ��pH������D����ȷ��
�ʴ�Ϊ��BD��
(2)���ܹ���ԭ��أ��Ҳ��ܹ���ԭ��أ���ԭ��ظ����Ľ������ٱ���ʴ����������ͬʱ���ڣ����ձ��в������ݵ��ٶȣ���>�ң�
�ʴ�Ϊ��>��
(3)���У�ͭ�缫�������ӵõ��������������缫��ӦʽΪ2H++2e=H2�������ݵ缫��Ӧʽ֪��ͨ�����ӵ����ʵ���=![]() ��2 = 0.1mol=0.1NA������ͨ�����ߵĵ�����ĿΪ6.02��1022��
��2 = 0.1mol=0.1NA������ͨ�����ߵĵ�����ĿΪ6.02��1022��
�ʴ�Ϊ��6.02��1022��
(4)ϡ�ͺ������ӵ����ʵ���Ϊ1L��0.1molL1 = 0.1 mol�����������������ӵ����ʵ���Ϊ![]() ��2=0.1 mol������ԭ��Һ�������ӵ����ʵ���Ϊ0.2mol��ԭ��Һ�������ӵ�Ũ��Ϊ
��2=0.1 mol������ԭ��Һ�������ӵ����ʵ���Ϊ0.2mol��ԭ��Һ�������ӵ�Ũ��Ϊ![]() = 2mol/L��һ����������к�����������,����ԭ��Һ��ϡ�����Ũ��Ϊ1molL1��
= 2mol/L��һ����������к�����������,����ԭ��Һ��ϡ�����Ũ��Ϊ1molL1��
�ʴ�Ϊ��1molL1��
��5����֪Fe+2Fe3+�T3Fe2+�����ݷ�Ӧ��֪FeӦΪ������ʧ���ӱ�������������ΪC��Cu�ȣ�������Fe3+�õ�������Fe2+���������Һ����Fe3+��
װ��ͼΪ ��̼��Ϊ������������Fe3+�õ�������Fe2+����缫��ӦΪ��2Fe3++2e-�T2Fe2+��FeΪ������ʧ���ӱ���������缫��ӦΪ��Fe-2e-�TFe2+���ʴ�Ϊ��
��̼��Ϊ������������Fe3+�õ�������Fe2+����缫��ӦΪ��2Fe3++2e-�T2Fe2+��FeΪ������ʧ���ӱ���������缫��ӦΪ��Fe-2e-�TFe2+���ʴ�Ϊ��
�ʴ�Ϊ�� ��Cu��2Fe3++2e-=2Fe2+��Fe��Fe-2e-=Fe2+��
��Cu��2Fe3++2e-=2Fe2+��Fe��Fe-2e-=Fe2+��
��6������ܷ�ӦΪ��8Li+3SOCl2=6LiCl+Li2SO3+2S����Li��0�����ߵ�+1�ۣ�ʧ���ӷ���������Ӧ����缫��ӦʽΪ��Li-e-=Li+�����﮵缫����Դ�ĸ�����ʯī��������
�ʴ�Ϊ��ʯī��Li-e-=Li+��