题目内容
【题目】用NA表示阿伏伽德罗常数值,下列叙述中正确的是
A. 5.6g铁在足量的O2中燃烧,转移的电子数为0.3NA
B. 18g H218O和D2O的混合物中,所含中子数为9NA
C. 1molFe分别与足量的稀硫酸和稀硝酸反应转移电子数均为2 NA
D. 0.4 mol NH3与0.6 mol O2在催化剂的作用下充分反应,得到NO的分子数为0.4NA
【答案】B
【解析】
A. 5.6g铁的物质的量是0.1mol,Fe在足量的O2中燃烧生成Fe3O4,每3molFe反应,转移8mol电子,则0.1molFe发生反应转移的电子数小于0.3NA,A错误;
B.H218O和D2O的分子中含有的中子数都是10个,若18g完全是 H218O,含有的中子数为![]() =9NA;若完全为D2O,则其中含有的中子数为
=9NA;若完全为D2O,则其中含有的中子数为![]() =9NA,故18g H218O和D2O的混合物中,所含中子数也一定为9NA,B正确;
=9NA,故18g H218O和D2O的混合物中,所含中子数也一定为9NA,B正确;
C. Fe为变价金属,与硫酸反应产生Fe2+,1molFe转移2NA个电子;若与HNO3反应,由于硝酸具有强的氧化性,会将Fe氧化为Fe3+,1mol反应后转移3NA电子,C错误;
D. NH3与O2在催化剂作用下发生反应:4NH3+5O2![]() 4NO+6H2O,但该反应为可逆反应,反应物不能完全转化为生成物,因此充分反应后得到NO的分子数小于0.4NA,D错误;
4NO+6H2O,但该反应为可逆反应,反应物不能完全转化为生成物,因此充分反应后得到NO的分子数小于0.4NA,D错误;
故合理选项是B。

【题目】下表是元素周期表的一部分,表中字母分别代表一种元素。回答下列问题。
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | a | b | c | d | ||||
3 | e | f | g | x | y | z |
(1)表中所标元素,最活泼的金属元素形成简单离子符号为____;最不活泼的元素的原子结构示意图为 _____;其中一种元素的气态氢化物与其最高价氧化物的水化物可直接化合生成一种盐,该盐是_______。
(2)写出两种满足下列条件的物质______(写化学式)。
①由c、x、e组成的;②含有共价键的离子化合物。
(3)g、x、y的气态氢化物,最稳定的是______(填化学式)。
(4)表中元素的最高价氧化物的水化物中:酸性最强的是______(填化学式,下同);碱性最强的是_______,这两种物质反应的离子方程式为_________。
(5)推测元素的非金属性:a ______ g(填“>”或“<”)。利用图装置设计实验,证明推测结论。
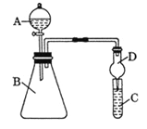
①仪器A的名称为___________,干燥管D的作用是______________。
②填空。
装置内试剂 | C中发生反应的化学方程式 | ||
A | B | C | |
稀硫酸 | 碳酸钠 | _______ | _______ |



