题目内容
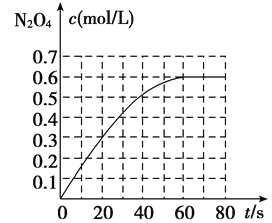
【题目】298 K时,在2 L固定体积的密闭容器中,发生可逆反应:2NO2(g) ![]() N2O4(g) ΔH=-a kJ/mol(a>0)。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,若反应在398 K进行,某时刻测得n(NO2)=0.6 mol,n(N2O4)=1.2 mol,则此时,下列大小关系正确的是( )
N2O4(g) ΔH=-a kJ/mol(a>0)。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,若反应在398 K进行,某时刻测得n(NO2)=0.6 mol,n(N2O4)=1.2 mol,则此时,下列大小关系正确的是( )
A. v(正)>v(逆)
B. v(正)<v(逆)
C. v(正)=v(逆)
D. v(正)、v(逆)大小关系不确定
【答案】B
【解析】试题分析:根据图示可知,在298K时,当反应达到平衡时c(N2O4)=0.6mol/L,由于平衡时,N2O4的浓度为NO2的2倍,则平衡时c(NO2)=0.3mol/L,则该温度下的化学平衡常数K= c(N2O4)/ c2(NO2)= 0.6mol/L÷(0.3mol/L)2=6.67L/mol;由于2NO2(g)![]() N2O4(g) △H=-akJ/mol(a>0)的正反应是放热反应,升高温度,化学平衡向吸热的逆反应方向移动,所以若反应在398K进行,反应达到平衡时的化学平衡常数K1<6.67。若反应在398K进行,某时刻测得n(NO2)=0.3mol/L、n(N2O4)=0.6mol/L,则Q= c(N2O4)/ c2(NO2)= 0.6mol/L÷(0.3mol/L)2=6.67L/mol,说明反应未处于平衡状态,反应逆向进行,因此v(正)<v(逆),选项B正确。
N2O4(g) △H=-akJ/mol(a>0)的正反应是放热反应,升高温度,化学平衡向吸热的逆反应方向移动,所以若反应在398K进行,反应达到平衡时的化学平衡常数K1<6.67。若反应在398K进行,某时刻测得n(NO2)=0.3mol/L、n(N2O4)=0.6mol/L,则Q= c(N2O4)/ c2(NO2)= 0.6mol/L÷(0.3mol/L)2=6.67L/mol,说明反应未处于平衡状态,反应逆向进行,因此v(正)<v(逆),选项B正确。

练习册系列答案
相关题目