题目内容
15.钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2═2Fe(OH)2.以下说法正确的是( )| A. | 负极发生的反应为:Fe-2e-═Fe2+ | |
| B. | 正极发生的反应为:2H2O+O2+2e-═4OH- | |
| C. | 钢铁发生的是析氢腐蚀 | |
| D. | 钢柱在水下部分比在空气与水交界处更容易腐蚀 |
分析 根据原电池的定义、原电池的电极反应式、以及氧气的溶解度判断,由于钢铁在潮湿的空气中会被腐蚀发生的原电池反应为:2Fe+2H2O+O2═2Fe(OH)2,发生的吸氧腐蚀,原电池中负极发生氧化反应,正极发生还原反应,据此分析判断.
解答 解:钢铁中含有铁和碳,在潮湿的环境中构成原电池,铁作负极,碳作正极.
A、根据反应方程式知,负极反应式为Fe-2e-Fe2+,故A正确;
B、正极是氧气得电子生成氢氧根离子,电极反应为:2H2O+O2+4e-=4OH-,故B错误;
C、根据正极反应可知,发生的是吸氧腐蚀,故C错误;
D、氧气在水中的溶解度较小,在水下部分比在空气与水交界处更难腐蚀,故D错误.
故选A.
点评 本题考查了金属的腐蚀与防护,明确形成原电池的条件及原电池原理是解本题关键,会根据环境确定钢铁发生吸氧腐蚀还是析氢腐蚀,会书写电极反应式,为学习难点.

练习册系列答案
相关题目
5.工业上用金红石(主要成分为TiO2)制金属钛,可通过以下反应进行:
①TiO2+2C+2Cl2 $\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO;
②TiCl4+2Mg$\frac{\underline{\;氩气\;}}{\;}$ Ti+2MgCl2;
设NA为阿伏伽德罗常数,对于上述两个反应的叙述中,正确的是( )
①TiO2+2C+2Cl2 $\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO;
②TiCl4+2Mg$\frac{\underline{\;氩气\;}}{\;}$ Ti+2MgCl2;
设NA为阿伏伽德罗常数,对于上述两个反应的叙述中,正确的是( )
| A. | 两个反应都是置换反应 | |
| B. | 每生成1mol金属Ti,②中转移电子数为2NA | |
| C. | ①中TiO2作氧化剂 | |
| D. | ②中氩气作保护气,可防止金属Ti被氧化 |
6.除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能到达试题目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 蒸馏 |
| D | 溴乙烷(乙醇) | 蒸馏水 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
10.下列说法正确的是( )
| A. | 由H原子形成1 mol H-H键要吸收能量 | |
| B. | 所有燃烧的反应都是放热反应 | |
| C. | NaOH溶于水是放热反应 | |
| D. | 吸热反应是能量降低的反应 |
20.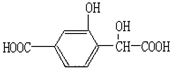 某有机物的结构简式如图所示,1mol的该有机物分别和足量的Na、NaOH、NaHCO3反应时,消耗三种物质的物质的量之比是( )
某有机物的结构简式如图所示,1mol的该有机物分别和足量的Na、NaOH、NaHCO3反应时,消耗三种物质的物质的量之比是( )
 某有机物的结构简式如图所示,1mol的该有机物分别和足量的Na、NaOH、NaHCO3反应时,消耗三种物质的物质的量之比是( )
某有机物的结构简式如图所示,1mol的该有机物分别和足量的Na、NaOH、NaHCO3反应时,消耗三种物质的物质的量之比是( )| A. | 1:1:1 | B. | 1:1:2 | C. | 4:3:2 | D. | 2:3:2 |
7.下列指定类别的化合物的同分异构体数目最多的是(不考虑立体异构)( )
| A. | 丁烷 | B. | 丁烯 | C. | 丁醇 | D. | 丁酸 |
5.一定条件下存在反应:H2(g)+I2(g)?2HI(g)△H<0,现有三个相同的1L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,按下列配比充入气体,700℃条件下开始反应,达到平衡时,下列说法正确的是( )
①在Ⅰ中充入1mol H2和1mol I2(g)
②在Ⅱ中充入2mol HI(g)
③在Ⅲ中充入2mol H2和2mol I2(g)
①在Ⅰ中充入1mol H2和1mol I2(g)
②在Ⅱ中充入2mol HI(g)
③在Ⅲ中充入2mol H2和2mol I2(g)
| A. | 容器Ⅰ、Ⅱ中正反应速率相同 | |
| B. | 容器Ⅰ、Ⅲ中反应的平衡常数相同 | |
| C. | 容器Ⅰ中的气体颜色比容器Ⅱ中的气体颜色深 | |
| D. | 容器Ⅰ中H2的转化率与容器Ⅱ中HI的转化率之和等于1 |
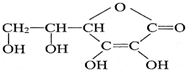 ,它的分子式是C6H8O6.在维生素C溶液中滴入少量酸性KMnO4溶液,可观察到的现象是酸性高锰酸钾颜色褪去,说明维生素C具有还原性.
,它的分子式是C6H8O6.在维生素C溶液中滴入少量酸性KMnO4溶液,可观察到的现象是酸性高锰酸钾颜色褪去,说明维生素C具有还原性.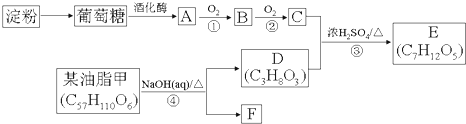
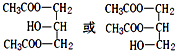 .
. .
.