题目内容
20.设NA为阿伏加德罗常数,则下列说法正确的是( )| A. | 1mol羟基与17g NH3所含电子数都为10NA | |
| B. | 1molCl2溶于水的过程中有NA个电子转移 | |
| C. | 1molC(金刚石)中σ 键的数目为2NA | |
| D. | 适量铜粉溶解于1L 0.5 mol/L稀硝酸中,当生成2.24L NO时,溶液中氮原子数为0.4NA |
分析 A、羟基没有发生电子的转移,1mol羟基含有9mol电子;
B、氯气与水的反应为可逆反应;
C、金刚石中每个σ键由两个碳原子形成,每个碳原子形成四个σ键,所以含有σ键2mol;
D、根据3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O及气体是否在标准状况下来分析.
解答 解:A、1mol羟基含有9mol电子,17g氨气的物质的量为1mol,含有10mol电子,二者含有的电子数不相等,故A错误;
B、氯气与水的反应为可逆反应,不能进行彻底,故1mol氯气转移的电子的个数小于NA个,故B错误;
C、1mol金刚石中含1molC原子,而每个σ键由两个碳原子形成,每个碳原子形成四个σ键,所以含有σ键2mol,即2NA个,故C正确;
D、若为标准状况,由3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O可计算出溶液中氮原子,但不知是否为标准状况,则无法利用NO的体积来计算其物质的量,故D错误.
故选C.
点评 本题考查有关物质的量及阿伏伽德罗常数的计算,明确电子数等于质子数、物质的化学键、电极反应式及电极材料是解答的关键,并注意标况下物质的状态来解答.

练习册系列答案
相关题目
14.己知红磷转化为白磷需要吸收热量.
①4P(s,红)+502(g)═2P205(s)△H1
②4P(s,白)+502(g)═2P205(s)△H2
则△H1与△H2的关系正确的是( )
①4P(s,红)+502(g)═2P205(s)△H1
②4P(s,白)+502(g)═2P205(s)△H2
则△H1与△H2的关系正确的是( )
| A. | △H1=△H2 | B. | △H1>△H2 | C. | △H1<△H2 | D. | 无法确定 |
8.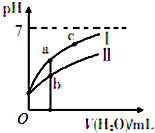 已知下表为25℃时某些弱酸的电离平衡常数;如图表示常温时,稀释CH3COOH、HC1O两种酸的稀溶液时,溶液pH随加水量的变化.
已知下表为25℃时某些弱酸的电离平衡常数;如图表示常温时,稀释CH3COOH、HC1O两种酸的稀溶液时,溶液pH随加水量的变化.
(1)图象中,曲线Ⅰ表示的酸是CH3COOH(填化学式);起始时,c(CH3COOH)<c(HClO)
(填“>”、“<”、“=”).
(2)a、b、c三点中,水的电离程度由大到小的顺序是c>a>b(用编号表示).
(3)25℃时,NaClO溶液的水解平衡常数Kh=$\frac{1}{3}$×10-6mol•L-1.
(4)向NaClO溶液中通入少量CO2的离子方程式为ClO-+CO2+H2O═HClO+HCO3-.
 已知下表为25℃时某些弱酸的电离平衡常数;如图表示常温时,稀释CH3COOH、HC1O两种酸的稀溶液时,溶液pH随加水量的变化.
已知下表为25℃时某些弱酸的电离平衡常数;如图表示常温时,稀释CH3COOH、HC1O两种酸的稀溶液时,溶液pH随加水量的变化.| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | K$_{{a}_{1}}$a1=4.4×10-7K$_{{a}_{2}}$a2=4.7×10-11 |
(填“>”、“<”、“=”).
(2)a、b、c三点中,水的电离程度由大到小的顺序是c>a>b(用编号表示).
(3)25℃时,NaClO溶液的水解平衡常数Kh=$\frac{1}{3}$×10-6mol•L-1.
(4)向NaClO溶液中通入少量CO2的离子方程式为ClO-+CO2+H2O═HClO+HCO3-.
15.下列变化中涉及化学变化的是( )
(1)爆竹燃放 (2)碘的升华
(3)金属钝化 (4)铝热反应
(5)干冰汽化(6)加热氯化铵
(7)甘油加水作护肤剂 (8)明矾净水
(9)蜂蚁螫咬后涂稀氨水可以减痛
(10)医用酒精可用于皮肤消毒
(11)烹鱼时加入少量的料酒和食醋可减少腥味
(12)橡胶老化 (13)用四氯化碳可擦去圆珠笔油渍
(14)蛋白质的盐析.
(1)爆竹燃放 (2)碘的升华
(3)金属钝化 (4)铝热反应
(5)干冰汽化(6)加热氯化铵
(7)甘油加水作护肤剂 (8)明矾净水
(9)蜂蚁螫咬后涂稀氨水可以减痛
(10)医用酒精可用于皮肤消毒
(11)烹鱼时加入少量的料酒和食醋可减少腥味
(12)橡胶老化 (13)用四氯化碳可擦去圆珠笔油渍
(14)蛋白质的盐析.
| A. | (1)(3)(4)(5)(7)(12)(13) | B. | (2)(4)(5)(7)(12)(13)(14) | ||
| C. | (2)(5)(7)(13)(14) | D. | 以上选项均不正确 |
5.下列关于元素周期表与化学键的知识叙述错误的是( )
| A. | 在周期表中过渡元素可作为催化剂 | |
| B. | 化学键可以使离子结合,也可以使原子结合 | |
| C. | 常温常压下,相同体积的O2和O3具有相同的分子数 | |
| D. | F2、Cl2、Br2、I2共价键逐渐增强,熔点依次升高 |
9.NA代表阿伏加德罗常数的值.下列有关叙述正确的是( )
| A. | 标准状况下,2.24LC6H14中含有1.9NA个共用电子对 | |
| B. | 7.8gNa2O2固体中含阴离子数目为0.1NA | |
| C. | 含36.5gHCl的浓盐酸与足量的二氧化锰作用,能产生0.25NA个氯气分子 | |
| D. | 5.6gFe与足量的氯气反应转移的电子数目为0.2NA |
10.下列物质中既含有非极性键,又含有极性键的是( )
| A. | CH4 | B. | Na2O2 | C. | C2H5OH | D. | H2O |