题目内容
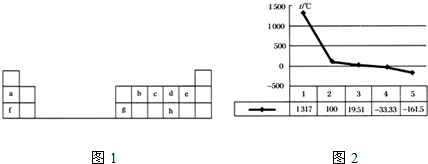
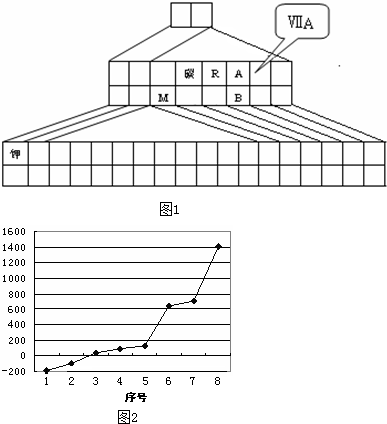
如图1是元素周期表的另一种画法--三角形元素周期表的一部分,图上标有第ⅦA族和碳、钾两种元素的位置.回答下列问题:
(1)在图1中将过渡元素所在的位置“涂黑”.
(2)R的第一电离能 A的第一电离能(填大于、小于或等于);写出铷元素原子的外围电子排布式 ;
(3)R的氢化物在A的氢化物中溶解度极大,原因是 ;A的氢化物比B的氢化物热稳定性强,原因是 .
(4)图中A、B两元素形成的离子B2
中,B元素呈现最高价,B原子位于由A原子组成的四面体的中心,且所有原子的最外层电子均满足8电子结构.该离子可能具有的化学性质是 ,依据是 .
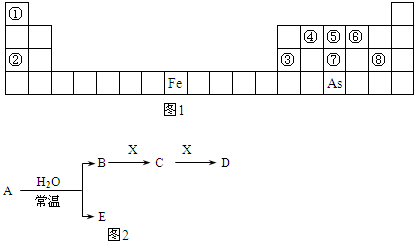
(5)第三周期8种元素按单质熔点(℃)高低的顺序如图2,(已知序号“1”代表Ar),其中序号“8”代表 (填元素符号);其中电负性最大的是 (填下图中的序号).
(6)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同.CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键.从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键的原因 .

(1)在图1中将过渡元素所在的位置“涂黑”.
(2)R的第一电离能
(3)R的氢化物在A的氢化物中溶解度极大,原因是
(4)图中A、B两元素形成的离子B2
| A | 2- 8 |
(5)第三周期8种元素按单质熔点(℃)高低的顺序如图2,(已知序号“1”代表Ar),其中序号“8”代表
(6)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同.CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键.从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键的原因
分析:三角形元素周期表的实质是将原周期表的空隙部分进行了删除形成的,与原元素周期表没有本质的区别,所以表中R为氮,A为氧,M为铝,B为硫,在第四周期之后的ⅡA和ⅢA之间为过渡元素,根据元素周期表的结构和元素所在周期表中的位置,结合元素周期律的有关递变规律以及对应元素化合物的性质解答该题.
解答:解:三角形元素周期表的实质是将原周期表的空隙部分进行了删除形成的,与原元素周期表没有本质的区别,所以表中R为氮,A为氧,M为铝,B为硫,在第四周期之后的ⅡA和ⅢA之间为过渡元素,
(1)三角形元素周期表的实质是将原周期表的空隙部分进行了删除形成的,与原元素周期表没有本质的区别,在第四周期之后的ⅡA和ⅢA之间为过渡元素,
故答案为: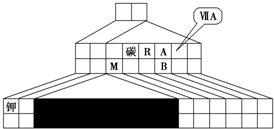 ;
;
(2)R为N,A为O,N原子的3p电子半满,为稳定结构,第一电离能大于A,铷元素原子的外围电子排布式为5s1,故答案为:大于;5s1;
(3)因氢键影响溶解性,化学键影响稳定性,则NH3是极性分子,水是极性分子,根据相似相溶原理,NH3易溶于水,且NH3与水分子间会形成氢键,增大溶解性,
水中H-O键的键长短,键能大,稳定性强,
故答案为:NH3是极性分子,水是极性分子,根据相似相溶原理,NH3易溶于水,且NH3与水分子间会形成氢键,增大溶解性;水中H-O键的键长短,键能大,稳定性强;
(4)A、B两元素形成的离子B2A82-中为S2082-,B原子位于由A原子组成的四面体的中心,则离子中含有-O-O-键,即过氧键,应具有氧化性,
故答案为:氧化性;离子结构中存在-O-O-(部分氧元素呈-1价亦可);
(5)第三周期8种元素,Si为原子晶体,熔点最高,则8为Si,Cl的非金属性最强,电负性最大,分子晶体中相对分子质量越大,熔沸点越大,图中2为Cl,
故答案为:Si;2;
(6)CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键,是因Si原子比C原子半径大,Si、O原子间距离较大,P-P轨道肩并肩重叠程度较小,不能形成上述稳定的π键,故答案为:Si原子比C原子半径大,Si、O原子间距离较大,P-P轨道肩并肩重叠程度较小,不能形成上述稳定的π键.
(1)三角形元素周期表的实质是将原周期表的空隙部分进行了删除形成的,与原元素周期表没有本质的区别,在第四周期之后的ⅡA和ⅢA之间为过渡元素,
故答案为:
 ;
;(2)R为N,A为O,N原子的3p电子半满,为稳定结构,第一电离能大于A,铷元素原子的外围电子排布式为5s1,故答案为:大于;5s1;
(3)因氢键影响溶解性,化学键影响稳定性,则NH3是极性分子,水是极性分子,根据相似相溶原理,NH3易溶于水,且NH3与水分子间会形成氢键,增大溶解性,
水中H-O键的键长短,键能大,稳定性强,
故答案为:NH3是极性分子,水是极性分子,根据相似相溶原理,NH3易溶于水,且NH3与水分子间会形成氢键,增大溶解性;水中H-O键的键长短,键能大,稳定性强;
(4)A、B两元素形成的离子B2A82-中为S2082-,B原子位于由A原子组成的四面体的中心,则离子中含有-O-O-键,即过氧键,应具有氧化性,
故答案为:氧化性;离子结构中存在-O-O-(部分氧元素呈-1价亦可);
(5)第三周期8种元素,Si为原子晶体,熔点最高,则8为Si,Cl的非金属性最强,电负性最大,分子晶体中相对分子质量越大,熔沸点越大,图中2为Cl,
故答案为:Si;2;
(6)CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键,是因Si原子比C原子半径大,Si、O原子间距离较大,P-P轨道肩并肩重叠程度较小,不能形成上述稳定的π键,故答案为:Si原子比C原子半径大,Si、O原子间距离较大,P-P轨道肩并肩重叠程度较小,不能形成上述稳定的π键.
点评:本题考查位置结构性质的相互关系及应用,题目难度不大,注意把握元素周期律的主要内容,本题关键之处在于理解三角形元素周期表的实质是将原周期表的空隙部分进行了删除形成的,与原元素周期表没有本质的区别.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目