题目内容
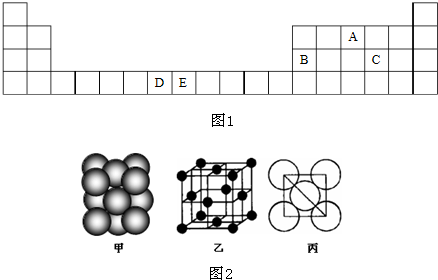
如图,是元素周期表的框架:
(1)周期表中元素①和元素⑤的最高价氧化物对应的水化物酸性强弱顺序是:
(2)元素③、④的最高价氧化物对应的水化物之间可以发生化学反应,写出反应的离子方程式:
(3)重金属元素⑦的盐溶液都有毒,但生活中仍可安全的使用铜器皿,其原因是
| ① | ② | ||||||||||||||||
| ③ | ④ | ⑤ | ⑥ | ||||||||||||||
| ⑦ | |||||||||||||||||
HNO3
HNO3
>H2SiO3
H2SiO3
(用含氧酸的化学式表示).元素②和元素⑥的氢化物的熔、沸点高低顺序是HF
HF
>HCl
HCl
(用氢化物的化学式表示).(2)元素③、④的最高价氧化物对应的水化物之间可以发生化学反应,写出反应的离子方程式:
OH-+Al(OH)3=AlO2-+2H2O
OH-+Al(OH)3=AlO2-+2H2O
;元素⑤的单质被誉为“信息革命的催化剂”,工业上可以用它的氧化物在一定条件下来制取,写出反应的化学方程式SiO2+2C
Si+2CO↑
| ||
SiO2+2C
Si+2CO↑
.
| ||
(3)重金属元素⑦的盐溶液都有毒,但生活中仍可安全的使用铜器皿,其原因是
金属铜化学性质不活泼
金属铜化学性质不活泼
.铜器皿长期放置表面上往往会产生一层铜绿,用稀硫酸可以将其清除,写出反应的离子方程式Cu2(OH)2CO3+4H+=2Cu2++3H2O+CO2↑
Cu2(OH)2CO3+4H+=2Cu2++3H2O+CO2↑
.分析:根据元素周期表的结构及元素在周期表中的位置知,①②③④⑤⑥⑦分别是N、F、Na、Al、Si、Cl、Cu元素,
(1)同一周期元素中,元素的非金属性随着原子序数的增大而增强,同一主族元素中,元素的非金属性随着原子序数的增大而减弱,元素的非金属性越强,其最高价氧化物的水化物酸性越强;根据HF分子之间存在氢键分析解答;
(2)元素③的最高价氧化物的水化物是NaOH,④的最高价氧化物对应的水化物是Al(OH)3,氢氧化铝能溶于氢氧化钠溶液生成偏铝酸钠;
元素⑤的单质是Si单质,工业上用二氧化硅和碳在高温下制取硅单质;
(3)重金属元素⑦是Cu,铜性质不活泼;铜绿的成分是碱式碳酸铜,铜绿能和稀硫酸反应生成硫酸铜、二氧化碳和水.
(1)同一周期元素中,元素的非金属性随着原子序数的增大而增强,同一主族元素中,元素的非金属性随着原子序数的增大而减弱,元素的非金属性越强,其最高价氧化物的水化物酸性越强;根据HF分子之间存在氢键分析解答;
(2)元素③的最高价氧化物的水化物是NaOH,④的最高价氧化物对应的水化物是Al(OH)3,氢氧化铝能溶于氢氧化钠溶液生成偏铝酸钠;
元素⑤的单质是Si单质,工业上用二氧化硅和碳在高温下制取硅单质;
(3)重金属元素⑦是Cu,铜性质不活泼;铜绿的成分是碱式碳酸铜,铜绿能和稀硫酸反应生成硫酸铜、二氧化碳和水.
解答:解:根据元素周期表的结构及元素在周期表中的位置知,①②③④⑤⑥⑦分别是N、F、Na、Al、Si、Cl、Cu元素,
(1)同一周期元素中,元素的非金属性随着原子序数的增大而增强,同一主族元素中,元素的非金属性随着原子序数的增大而减弱,元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性N>C>Si,所以其最高价含氧酸的酸性强弱顺序是HNO3>H2SiO3;HF分子之间存在氢键,所以HF的熔沸点大于HCl,
故答案为:HNO3;H2SiO3;HF;HCl;
(2)元素③的最高价氧化物的水化物是NaOH,④的最高价氧化物对应的水化物是Al(OH)3,氢氧化铝能溶于氢氧化钠溶液生成偏铝酸钠,离子反应方程式为:OH-+Al(OH)3=AlO2-+2H2O;
元素⑤的单质是Si单质,工业上用二氧化硅和碳在高温下制取硅单质,反应方程式为:SiO2+2C
Si+2CO↑;
故答案为:OH-+Al(OH)3=AlO2-+2H2O;SiO2+2C
Si+2CO↑;
(3)重金属元素⑦是Cu,铜性质不活泼,所以生活中仍可安全的使用铜器皿;
铜绿的成分是碱式碳酸铜,铜绿能和稀硫酸反应生成硫酸铜、二氧化碳和水,离子反应方程式为:Cu2(OH)2CO3+4H+=2Cu2++3H2O+CO2↑,
故答案为:金属铜化学性质不活泼; Cu2(OH)2CO3+4H+=2Cu2++3H2O+CO2↑.
(1)同一周期元素中,元素的非金属性随着原子序数的增大而增强,同一主族元素中,元素的非金属性随着原子序数的增大而减弱,元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性N>C>Si,所以其最高价含氧酸的酸性强弱顺序是HNO3>H2SiO3;HF分子之间存在氢键,所以HF的熔沸点大于HCl,
故答案为:HNO3;H2SiO3;HF;HCl;
(2)元素③的最高价氧化物的水化物是NaOH,④的最高价氧化物对应的水化物是Al(OH)3,氢氧化铝能溶于氢氧化钠溶液生成偏铝酸钠,离子反应方程式为:OH-+Al(OH)3=AlO2-+2H2O;
元素⑤的单质是Si单质,工业上用二氧化硅和碳在高温下制取硅单质,反应方程式为:SiO2+2C
| ||
故答案为:OH-+Al(OH)3=AlO2-+2H2O;SiO2+2C
| ||
(3)重金属元素⑦是Cu,铜性质不活泼,所以生活中仍可安全的使用铜器皿;
铜绿的成分是碱式碳酸铜,铜绿能和稀硫酸反应生成硫酸铜、二氧化碳和水,离子反应方程式为:Cu2(OH)2CO3+4H+=2Cu2++3H2O+CO2↑,
故答案为:金属铜化学性质不活泼; Cu2(OH)2CO3+4H+=2Cu2++3H2O+CO2↑.
点评:本题考查了元素周期表和元素周期律的综合应用,正确推断元素并结合元素周期律来分析解答即可,注意高温下二氧化硅和碳反应生成一氧化碳而不是二氧化碳,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目