题目内容
【题目】某研究小组为了探究一种无机矿物盐X(仅含四种元素)的组成和性质,设计并完成如下实验:
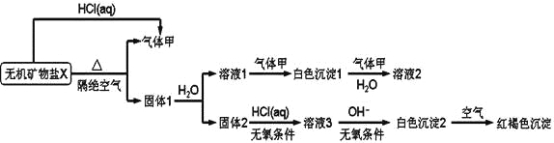
另取10.80gX在惰性气流中加热至完全分解,得到6.40g固体1。请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图_______,
写出气体甲的电子式________。
(2)X的化学式是____,在惰性气流中加热X至完全分解的化学方程式为_______________。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是________________。
(用化学方程式表示)。
(4)一定条件下,气体甲与固体1中某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式____________________,并设计实验方案验证该反应的产物_________________________。
【答案】(1)![]() ;
;![]()
(2)CaFe(CO3)2;CaFe(CO3)2![]() CaO+FeO+2CO2↑
CaO+FeO+2CO2↑
(3)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(4)2FeO+CO2![]() Fe2O3+CO;取适量固体于试管中,加入盐酸溶解,滴入几滴KSCN溶液,若溶液变红色,说明产物中含有三价铁。
Fe2O3+CO;取适量固体于试管中,加入盐酸溶解,滴入几滴KSCN溶液,若溶液变红色,说明产物中含有三价铁。
【解析】试题分析:X能和HCl反应生成气体甲,隔绝空气加热X得到气体甲和固体1,且X和HCl(aq)反应也能得到甲,因此猜测X是碳酸盐,因为X加热易分解且能和酸反应生成CO2,那么甲为CO2,固体1溶于水得到溶液1和固体2,溶液1和二氧化碳反应生成白色沉淀1,白色沉淀1和二氧化碳、水反应生成溶液2,则白色沉淀1为碳酸盐、溶液2为碳酸氢盐;固体2和稀盐酸反应生成溶液3,且需要无氧条件,溶液3中加入碱在无氧条件下生成白色沉淀2,白色沉淀2被空气氧化生成红褐色沉淀,则白色沉淀2是Fe(OH)2,溶液3为FeCl2,X仅含4种元素,碳酸盐分解生成二氧化碳气体和两种氧化物,其中一种氧化物能溶于水,结合地壳的成分猜测固体1中成分为CaO、FeO,对应地,X应为CaFe(CO3)2,结合题中信息:10.80gX在惰性气流中加热至完全分解,得到6.40g固体1,经计算,确认X为CaFe(CO3)2,那么,溶液1是Ca(OH)2,白色沉淀1是CaCO3,溶液2是Ca(HCO3)2。
(1)白色沉淀1是CaCO3,碳酸钙中金属元素的原子核外有4个电子层、最外层有2个电子,所以Ca原子结构示意图为![]() ,气体甲是二氧化碳,二氧化碳的电子式为
,气体甲是二氧化碳,二氧化碳的电子式为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;
(2)通过以上分析知,X的化学式是CaFe(CO3)2,在惰性气流中加热X至完全分解生成二氧化碳和氧化钙、氧化亚铁,所以该反应的化学反应方程式为CaFe(CO3)2![]() CaO+FeO+2CO2↑,故答案为:CaFe(CO3)2;CaFe(CO3)2
CaO+FeO+2CO2↑,故答案为:CaFe(CO3)2;CaFe(CO3)2![]() CaO+FeO+2CO2↑;
CaO+FeO+2CO2↑;
(3)氢氧化亚铁不稳定,易被空气氧化生成红褐色氢氧化铁,所以白色沉淀2在空气中变成红褐色沉淀,反应方程式为4Fe(OH)2+2H2O+O2=4Fe(OH)3,故答案为:4Fe(OH)2+2H2O+O2=4Fe(OH)3;
(4)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,氧化亚铁具有还原性,能被二氧化碳氧化生成四氧化三铁或氧化铁,同时生成CO,反应方程式为2FeO+CO2![]() Fe2O3+CO(或生成Fe3O4),如果该反应发生,则生成固体中含有三价铁,将固体溶于稀盐酸生成铁离子,铁离子和KSCN溶液反应生成血红色物质而使溶液变红色,故答案为:2FeO+CO2
Fe2O3+CO(或生成Fe3O4),如果该反应发生,则生成固体中含有三价铁,将固体溶于稀盐酸生成铁离子,铁离子和KSCN溶液反应生成血红色物质而使溶液变红色,故答案为:2FeO+CO2![]() Fe2O3+CO(或生成Fe3O4);取适量固体于试管中,加入盐酸溶解,滴入几滴KSCN溶液,若溶液变红色,说明产物中含有三价铁。
Fe2O3+CO(或生成Fe3O4);取适量固体于试管中,加入盐酸溶解,滴入几滴KSCN溶液,若溶液变红色,说明产物中含有三价铁。

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】
A.在500 mL容量瓶中配制500 mL烧碱溶液 |
B.用移液管(或碱式滴定管)量取50.00 mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂 |
C.在天平上准确称取烧碱样品m g,在烧杯中加蒸馏水溶解 |
D.将物质的量浓度为c mol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1mL |
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2mL 请完成下列问题:
(1)正确的操作步骤是(填写字母)________→________→________→D→________.
(2)滴定管读数应注意_______________________.
(3)操作中锥形瓶下垫一张白纸的作用是___________________.
(4)操作D中液面应调整到________________________;尖嘴部分应____________.
(5)滴定到终点时锥形瓶内溶液的pH约为___________;终点时的颜色变化是________.
(6)若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响________(填“偏高”、“偏低”或“无影响”,其他操作均正确).
(7)该烧碱样品的纯度计算式是__________________.
【题目】某合金与铁的物理性质的比较见下表:
熔点(℃) | 密度/(g·cm-3) | 硬度(金 刚石为10) | 导电性 (银为100) | |
某合金 | 2 500 | 3.00 | 7.4 | 2.3 |
铁 | 1 535 | 7.86 | 4.5 | 17 |
还知该合金耐腐蚀、强度大,从以上性能看,该合金不适合做( )
A. 导线 B. 门窗框
C. 炉具 D. 飞机外壳