题目内容
下列说法正确的是( )
| A、碱性:LiOH>NaOH>KOH>RbOH |
| B、金属性:Rb>K>Na>Li |
| C、Rb不易与水反应放出H2 |
| D、和酸反应时Fe能失2个e-,Na失1个e-,所以Fe的金属性强于Na |
考点:金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:同主族元素从上到下,元素的金属性逐渐增强,对应的最高价氧化物的水化物的碱性逐渐增强,元素的金属性越强,对应的单质越活泼,注意金属性的强弱与失电子的难易有关,而与失电子的多少无关.
解答:
解:A.碱性LiOH<NaOH<KOH<RbOH,故A错误;
B.同主族元素从上到下,元素的金属性逐渐增强,金属性:Rb>K>Na>Li,故B正确;
C.金属性Rb>Na,由钠与水反应的性质可知Rb能与水发生剧烈反应,故C错误;
D.金属性的强弱与失电子的难易有关,而与失电子的多少无关,故D错误.
故选B.
B.同主族元素从上到下,元素的金属性逐渐增强,金属性:Rb>K>Na>Li,故B正确;
C.金属性Rb>Na,由钠与水反应的性质可知Rb能与水发生剧烈反应,故C错误;
D.金属性的强弱与失电子的难易有关,而与失电子的多少无关,故D错误.
故选B.
点评:本题考查同主族元素的性质的递变规律,侧重于碱金属的考查,为高频考点,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
具有相同的质子数和相同电子数的一组微粒是( )
| A、OH-、H2O、F- |
| B、H3O+、NH4+、Na+ |
| C、NH3、NH4+、F- |
| D、Cl-、HS-、S2- |
下列反应的离子方程式书写正确的是( )
| A、98.3%的硫酸加入到稀氢氧化钡溶液中:H+(aq)+OH-(aq)═H2O(aq);△H=-57.3kJ/mol |
| B、100mL 0.1mol?L-1的Na2CO3溶液中逐滴加入0.01mol CH3COOH:CO32-+2CH3COOH═CO2↑+2CH3COO-+H2O |
| C、铜片插入氯化铁溶液中:Cu+2Fe3+═Cu2++2Fe2+ |
| D、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O═AlO2-+4NH4+ |
下列各组物质中,全部属于纯净物的是( )
| A、福尔马林、白酒、食醋 |
| B、汽油、酒精、聚乙烯 |
| C、石炭酸、盐酸、冰醋酸 |
| D、甘油、乙醇钠、氯仿 |
对于反应IBr+H2O═HBr+HIO的说法正确的是( )
| A、IBr只作氧化剂 |
| B、IBr只作还原剂 |
| C、IBr既是还原剂又是氧化剂 |
| D、IBr既不是氧化剂也不是还原剂 |
下列离子能在溶液中大量共存的是( )
| A、K+,NO3-,MnO4-,NH4+ |
| B、Al3+,AlO2-,K+,SO42- |
| C、Mg2+,Cl-,Na+,OH- |
| D、Fe2+,H+,Cl-,NO3- |
下列各项实验的基本操作中,正确的是( )
| A、为了加快过滤速度,可用玻璃棒搅拌过滤器中的液体 |
| B、为了分离苯和四氯化碳的混合物,可用分液漏斗分液 |
| C、用碱式滴定管取23.10mL溴水 |
| D、用托盘天平称量11.7g氯化钠晶体 |
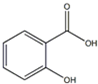 水杨酸具有防腐杀菌作用,还有祛除汗臭、止痒消肿、止痛消炎等功能,主要用于花露水、痱子水以及一些水类化妆品.水杨酸的结构简式如图所示,请回答下列问题.
水杨酸具有防腐杀菌作用,还有祛除汗臭、止痒消肿、止痛消炎等功能,主要用于花露水、痱子水以及一些水类化妆品.水杨酸的结构简式如图所示,请回答下列问题.